Конверсия - реагент
Cтраница 1
Конверсия реагентов в реакциях диспропорцйонирования ограничивается термодинамическим равновесием, однако выбор рабочих температур зависит от природы применяемого катализатора. Для диспропорцйонирования олефинов применяются катализаторы двух типов: гомогенные и гетерогенные. [1]
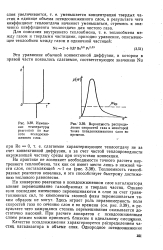 |
Изменение температуры реагентов по высоте псевдоожиженного слоя. [2] |
На конверсию реагентов в псевдоожиженном слое катализатора влияет перемешивание газообразных и твердых частиц. Однако если последние интенсивно перемешиваются в слое за счет гравитационных сил, то компоненты газовой фазы перемешиваться таким образом не могут. Здесь играет роль неравномерность поля скоростей газа по сечению слоя и во времени ( см. рис. 3.39), в результате чего кажущаяся степень перемешивания оказывается достаточно высокой. [3]
На конверсию реагентов в псевдоожиженном слое катализатора влияет перемешивание газообразных и твердых частиц. Однако если твердые частицы интенсивно перемешиваются в слое за счет гравитационных сил, то компоненты газовой фазы перемешиваться таким образом не могут. Здесь играет роль неравномерность поля скоростей газа по сечению слоя и во времени, в результате чего кажущаяся степень перемешивания оказывается достаточно высокой. [4]
Из-за малой степени конверсии реагентов и высоких температуры и давления при прямой гидратации этилена важнейшее значение имеют вопросы рециркуляции веществ и экономии энергии. Существующие схемы процессов заметно различаются, в особенности происхождением водяного пара, требуемого для синтеза, и степенью очистки целевого продукта. [5]
Таким образом, возможность увеличения конверсии реагентов, образующих азеотропы, при использовании повышенного или пониженного рабочего давления следует учитывать при выборе условий организации конкретных процессов. [6]
Выражение (1.22) устанавливает связь между конверсиями реагентов At и А ( и позволяет рассчитать неизвестную степень превращения другого вещества. [7]
Причем при постоянной нагрузке по сырью увеличивается степень конверсии реагентов. [8]
Правильное применение совмещения различных процессов позволяет повысить не только конверсию реагентов, но и выход целевых продуктов при меньших затратах энергии. [9]
Уравнения (7.5) и (7.8) можно объединить и затем вывести аналитически уравнение для конверсии реагента в реакторе идеального вытеснения. [10]
Реакция тормозится неконтролируемыми примесями в реагенте, и для поддержания требуемой 60 % - ной конверсии реагента необходимо обеспечить регулирование расхода катализатора. Процент конверсии измеряется рефрактометром. В измерительном канале имеется запаздывание только в системе отбора проб выходящего продукта, которое составляет 50 сек. Тепловыделение реакции мало, и температура легко поддерживается с точностью 0 25 С путем изменения температуры рубашки. [11]
Как видно из рис. 3.5, для целевого получения вещества В ] кроме высокой степени конверсии реагента А необходимо применение реактора полного смешения. Для целевого получения продукта В2 кроме понижения степени конверсии вещества А целесообразно использовать реактор идеального вытеснения или периодический. [12]
Для процессов, описываемых реак-пиями первого и псевдопервого порядка ( скорость превращения этилена при оксихлорировании), конверсии реагентов рассчитываются с удовлетворительной точностью с помощью двухфазной модели. Параметры модели определяются при этом исследованием холодных аппаратов. [13]
На основе дальнейшего анализа модели случайных слияний и распадов авторы [30] делают вывод о том, что степень конверсии реагента нечувствительна к деталям процесса перемешивания. При этом предполагалось, что оба реагента имеют одинаковые коэффициенты диффузии D. [14]
Подставляя значение Г в уравнения ( XII, 12) и ( XII, 13), получаем конверсию реагента в каталитическом реакторе. [15]
Страницы: 1 2 3 4