Конверсия - реагент
Cтраница 3
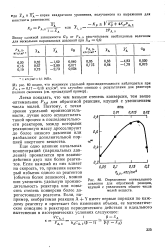
Для процессов, сочетающих прямое и окислительное хлорирование метана ( сбалансированная и комбинированная схемы), принципиальное значение имеет состав реакционного газа, который поступает на стадию окислительного хлорирования, который, в свою очередь, зависит от соотношения исходных метана и хлора. На рис. 23, а показаны степени конверсии реагентов и состав хлорметанов в процессе оксихлорирования в зависимости от мольного соотношения метана и хлора при прямом хлорировании. Газ, поступающий с прямого хлорирования на окислительное, содержит 35 % ( об.) метана. [31]
В предельном случае, при R -, на вход в реактор будет поступать бесконечно большой поток питания, состоящий из чистого реагента А. При этом, скорость химической реакции стремится к нулю и, следовательно, конверсия реагентов также стремится к нулю. [32]
При случайных колебаниях температуры в реакторе может заметно изменяться вязкость реакционной среды, а значит и регистрируемая электрическая мощность на валу мешалки. Таким образом, случайное изменение рабочей температуры является источником ложной информации о степени конверсии реагентов. [33]
Наличие газовых пузырей ( дискретной фазы) и равномерно-распределенных твердых частиц ( сплошная или эмульсионная фаза) обуславливает специфику взвешенного слоя, условия контакта газовой и твердой фазы. Очевидно, что проскок газа в виде таких пузырей монет свести нь нет все преимущества взвешенного слоя, резко уменьшить степень конверсии реагентов. До настоящего времени физическая модель взвешенного слоя остается практически неизученной. В литературе нет надежных данных, которые позволили бы определить объем газа, проходящего слой в виде пузырей, размер их, массообмен между сплошной и дискретной фазой. [34]
Реакцию проводят при 200 - 300 С с избытком аммиака или амина под давлением, необходимым для поддержания реакционной массы в жидком состоянии. При малой летучести кислоты и амида можно барботировать при атмосферном давлении аммиак, который одновременно выдувает образующуюся воду, способствуя высокой степени конверсии реагентов. Второй вариант обычно применяют и при производстве амидов из сложных эфиров, для чего требуется температура 50 - 100 С. [35]
Реакцию проводят при 200 - 300 С с избытком аммиака или амина под давлением, необходимым для поддержания реакционной массы в жидком состоянии. При малой летучести кислоты и амида можно барбо-тировать при атмосферном давлении аммиак, который одновременно выдувает образующуюся воду, способствуя высокой степени конверсии реагентов. Второй вариант обычно применяют и при производстве амидов из сложных эфиров, для чего требуется температура 50 - 100 С. [36]
Процессы, в которых альдольную конденсацию ( альдоли-зация) проводят отдельно от последующих реакций в специальном реакторе. Для этой стадии характерен низкая температура ( О-30 С), большая длительность ( 2 - 3 ч) и невысокая степень конверсии реагентов ( 10 - 40 %), вызванная как обратимостью реакции, так и стремлением предотвратить последовательные превращения целевых продуктов. Последнее обстоятельство делает также целесообразным использование реакторов, близких к модели идеального вытеснения, например змеевиковых аппаратов. [37]
Реакцию проводят при 150 - 200 С с избытком аммиака или амина под давлением, необходимым для поддержания реакционной массы в жидком состоянии. При малой летучести кислоты и амида можно барботировать при атмосферном давлении аммиак, который одновременно выдувает образующуюся воду, способствуя высокой степени конверсии реагентов. Второй вариант обычно применяют и при производстве амидов из сложных эфиров, для чего требуется температура 50 - 100 С. [38]
При этом особенно выгодно совмещать две реакции, одна из которых является экзотермической, а другая - эндотермической. В этом случае режим процесса в целом может приближаться к адиабатическому, в результате чего не только сокращаются энергетические затраты, но и повышается конверсия реагентов. Примером такого совмещения реакций может служить окислительное дегидрирование углеводородов при получении бутадиена-1 3, стирола и а-метилстирола. [39]
Аммиак и кислород в мольном соотношении 1: 1 подаются в реактор кипящего слоя RI, в котором при температуре 350 - 370 С и давлении до 5 атм происходит селективное окисление основного количества аммиака в закись азота. Выходящая из реактора кипящего слоя смесь, содержащая примерно по 1 % ( об.) остаточных аммиака и кислорода, попадает в реактор R2, где происходит конверсия остаточных реагентов с образованием закиси азота. Газ, выходящий из реактора R3, охлаждается и попадает в абсорбер А1, где происходит отмывка продукционного газа от аммиака. Остаточное содержание NO, в продукционном газе не превышает 40 ррт. [40]
 |
Определение оптимального. [41] |
Еще одно влияние начальных концентраций ( парциальных давлений) проявляется при взаимодействии двух или более реагентов. Если каждый из них влияет на скорость, то, применяя некоторый избыток одного из реагентов ( обычно более дешевого), можно или увеличить удельную производительность реактора или повысить степень конверсии более дорогостоящего реагента. [42]
Ур Урект, VpeKT / Vp составляет большую конечную величину. Тогда при некотором конечном времени пребывания реагентов в системе ( некоторой конечной интенсивности обмена системы с окружающей средой), в соответствии с исходными условиями, за счет химической реакции установится некоторая постоянная величина конверсии реагентов и соответствующие ей концентрации компонентов реакционной смеси. [43]
 |
Состав технических изобутиленсодержащих С4 - фракций ( вес. %. [44] |
Перечисленные особенности процесса синтеза ДМД определяют требования, предъявляемые к реакционному устройству. Конструкция последнего должна обеспечивать а) интенсивный массообмен между органической и водной фазами; б) поддержание заданной температуры в зоне реакции и съем избыточного тепла ( тепло реакции); в) время контакта фаз, необходимое для установленной конверсии реагентов. [45]
Страницы: 1 2 3 4