Равновесная конверсия
Cтраница 1
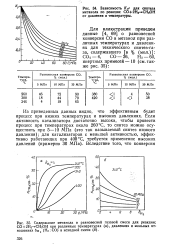
Равновесная конверсия по уравнениям ( 1) и ( 2) достигается при температуре около 500 С. [1]
На равновесные конверсии реакций с участием водорода боль -: шое влияние оказывают не только температура и давление ( они определяют величину K. N), но и мольное отношение водород: сырье - 6н2 - Последнее, как видно из данных табл. 80, может существенно изменять равновесную конверсию х при неизменных температуре и давлении. Поскольку технические процессы и гидрирования, и дегидрирования проводят, вводя водород в реакционную зону ( например, для поддержания стабильной активности катализатора), проиллюстрируем влия ние бн2 на х на конкретных примерах для гидрирования и дегидрирования. [2]
Определим возможную равновесную конверсию циклогек-сана. Из уравнения, справедливого при отсутствии бензола в исходной смеси ( см. разд. К дегидрирование возможно практически нацело. [3]
Указанными авторами приведены расчеты равновесных конверсии и концентраций этилового спирта при 150 - 400 п 50 - 200 ат. [4]
При постоянных температуре-и константе равновесия степень равновесной конверсии возрастает с понижением давления. Понижение парциального давления этилбензола при постоянной конверсии позволяет существенно снизить температуру дегидрирования. Так, 50 % - ная конверсия этилбензола в стирол при давлении 0 1 МПа и без инертных разбавителей достигается при 620 С, при давлении 0 01 МПа - при 505 С, а при разбавлении 20 объемами водяного пара и общем давлении 0 01 МПа - при 500 С. [5]
Для иллюстрации приведем данные [4, 69] о равновесной конверсии СО в метанол при различных температурах и давлениях для технического синтез-газа, содержавшего [ в % ( мол. [7]
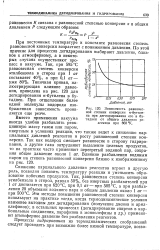 |
Зависимость равновесной степени конверсии - бутилена при дегидрировании его в бутадиен от общего давления реагентов при 860 К. [8] |
При постоянных температуре и константе равновесия степень равновесной конверсии возрастает с понижением давления. По этой причине для процессов дегидрирования выбирают давление, близкое к атмосферному, а в некоторых случаях осуществляют процесс в вакууме. Типичная кривая, иллюстрирующая влияние давления, приведена на рис. 120 для дегидрирования н-бутилена в бутадиен. При отщеплении более одной молекулы водорода изображенная зависимость проявляется еще резче. [9]
При постоянных температуре и константе равновесия степень равновесной конверсии возрастает с понижением давления. По этой причине для процессов дегидрирования выбирают давление, близкое к атмосферному, а в некоторых случаях осуществляют процесс в вакууме. Типичная кривая, иллюстрирующая влияние давления, приведена на рис. 116 для дегидрирования н-бутилена в бутадиен. При отщеплении более одной молекулы водорода изображенная зависимость проявляется еще резче. [10]
Из этих данных следует, что при атмосферном давлении равновесная конверсия дегидрирования невелика, даже при 900 К она не превышает 30 % ( мол. Снижение парциального давления н-бутиленов должно сдвинуть реакцию дегидрирования вправо. [11]
Как видно из приведенных данных, при одинаковых условиях равновесные конверсии дегидрирования н-бутиленов в бутадиен и смеси изоамиленов в изопрен мало отличаются. Так, при 800 К и атмосферном давлении для м - С4Н8 Кр 0 0102, а для ызо - СБН10 / ( р 0 0131; значения Х0 равны 10 0 и 11 4 % ( мол. [12]
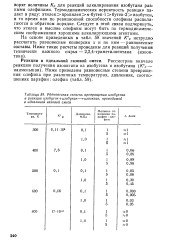 |
Равновесная степень превращения изобутена в реакции изобутен изобутан - изооктан, проводимой в идеальной газовой смеси. [13] |
На основе приведенных в табл. 58 значений К Р нетрудно рассчитать равновесные конверсии х и по ним - равновесные составы. [14]
В промышленных условиях при одностадийном дегидрировании парафинов в реактор подается парафин-олефиновая смесь, поэтому при расчетах равновесных конверсии дегидрирования нужно определять состав исходной смеси углеводородов, обеспечивающий теоретическую одностадийность и теоретически возможные выходы диенов. [15]
Страницы: 1 2 3 4