Равновесная конверсия
Cтраница 3
С повышением температуры процесса ( рис. 15) увеличивается константа равновесия и возрастает выход хлор-этенов. При температуре 200 С абсолютное большинство хлорэтанов имеют равновесную конверсию выше 90 %, а повышение температуры до 400 - 500 С делает практически необратимой и реакцию дегидрохлорирования 1 2-дихлорэтана. [31]
 |
Константы равновесия димеризации этилена и пропилена с образованием димеров различной структуры. [32] |
Нужно, однако, иметь в виду, что если димеризация проводится при относительно высокой температуре, так что значение К рр не превышает двух, то термодинамические ограничения по образованию димеров становятся особенно значительными и в-этом случае основным продуктом димеризации будет тот, для которого указанное значение наибольшее. В связи с этим при сопоставлении термодинамических расчетов и экспериментальных равновесных конверсии составов нужно учитывать, образуются ли только один димер или димеры разной структуры. [33]
Для предотвращения чрезмерного развития этих реакций обра - - тимые процессы дегидратации не следует доводить до высокой степени конверсии. В процессах образования кетена из уксусной кислоты происходит увеличение объема, и, следовательно, повышению равновесной конверсии способствует пониженное давление. При межмолекулярной дегидратации давление такого влияния не оказывает. [34]
Состав продуктов реакции является исключительно функцией температуры, давления и времени контакта, если сырье состоит из одного реагента. Если указанные переменные факторы действуют на концентрацию продуктов так, что глубина конверсии становится незначительной сравнительно с равновесной конверсией, то следует рассматривать только кинетику дальнейших реакций. Получаемые выходы продукта ограничиваются константой равновесия. [35]
На равновесные конверсии реакций с участием водорода боль -: шое влияние оказывают не только температура и давление ( они определяют величину K. N), но и мольное отношение водород: сырье - 6н2 - Последнее, как видно из данных табл. 80, может существенно изменять равновесную конверсию х при неизменных температуре и давлении. Поскольку технические процессы и гидрирования, и дегидрирования проводят, вводя водород в реакционную зону ( например, для поддержания стабильной активности катализатора), проиллюстрируем влия ние бн2 на х на конкретных примерах для гидрирования и дегидрирования. [36]
 |
Зависимость скорости экзотермической обратимой реакции dx / dr.| Диаграмма х - t для экзотермической обратимой реакции. - оптимальные температуры. - - - - - - - - равновесные конверсии. [37] |
Наличие максимума на кривых может быть объяснено следующим. Однако равновесная конверсия для экзотермических реакций с повышением температуры снижается. Поэтому при какой-то достаточно высокой температуре скорость реакции может стать равной нулю. Значит, при какой-то более низкой температуре она должна проходить через максимум. [38]
ДАС получают альдольной конденсацией ацетона. Реакция обратима, равновесная конверсия ацетона увеличивается с понижением температуры. [39]
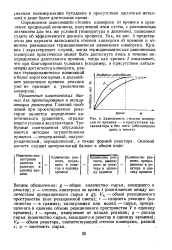 |
Зависимость степени конверсии от времени - в присутствии катализатора и без него ( обозначения даны в тексте. [40] |
Определение зависимости степени конверсии от времени и сравнение предельной величины, полученной этим путем, с равновесным значением для тех же условий ( температура и давление), позволяют судить об эффективности данного процесса. Так, на рис. 4 представлены два варианта зависимости степени конверсии от времени и отмечена равновесная термодинамически возможная конверсия. Кривая / характеризует случай, когда термодинамическая равновесная конверсия практически может быть достигнута лишь в течение неопределенно длительного времени, тогда как кривая 2 показывает, что при благоприятных условиях ( например, в присутствии катализатора) достигается конверсия, равная термодинамически возможной в более короткое время, и дальнейшее увеличение времени реакции уже не приведет к увеличению конверсии. [41]
Определение зависимости степени конверсии от времени и сравнение предельной величины, полученной этим путем, с равновесным значением для тех же условий ( температура и давление), позволяют судить об эффективности данного процесса. Так, на рис. 4 представлены два варианта зависимости степени конверсии от времени и отмечена равновесная термодинамически возможная конверсия. Кривая / характеризует случай, когда термодинамическая равновесная конверсия практически может быть достигнута лишь в течение неопределенно длительного времени, тогда как кривая 2 показывает, что при благоприятных условиях ( например, в присутствии катализатора) достигается конверсия, раь-ная термодинамически возможной в более короткое время, и дальнейшее увеличение времени реакции уже не приведет к увеличению конверсии. [42]
Для обратимых экзотермических реакций, сопровождающихся побочными процессами, определение оптимальных температур более сложно. То же относится и к обратимым эндотермическим реакциям. В последнем случае с ростом температуры возрастает не только скорость реакции, но и равновесная конверсия. [43]
Расчет температуры, соответствующей определенному значению Kf, дает относительную погрешность, равную относительной погрешности вычисления AFf. Так, если ошибка определения AFf составляет 1 00 ккал / моль, то, например, для пропана получаем погрешность 6Г К при температуре 500 К и только 9 6 К для циклогексана при 1000 К. На основании всего этого можно заключить, что наибольшее практическое значение расчета AF заключается в обеспечении основы для расчета температур, которые необходимы для достижения равновесной конверсии в интересующей нас реакции. [44]
При выбранных температуре и давлении производительность реактора зависит от скорости подачи реагентов. Уменьшение ее, хотя и ведет к увеличению степени конверсии, но снижает производительность единицы объема катализатора по спирту ввиду уменьшения средней скорости реакции. Оптимальная степень конверсии за один проход оказалась равной 4 - 4 5 % по олефину или 7 % по воде, что составляет около 60 % от равновесной конверсии. При таких условиях после охлаждения реакционной массы получается конденсат с 15 % спирта. Несмотря на малую степень конверсии за один проход через реактор, процесс прямой гидратации этилена и пропилена отличается высокой селективностью. Остальное количество олефина расходуется на образование эфира ( 2 %), полимеров ( 2 %) и небольшого количества ацетальдегида. Для спиртов С4 и выше прямая гидратация непригодна ввиду невыгодных условий равновесия и сильной полимеризации олефина. [45]
Страницы: 1 2 3 4