Конец - осаждение
Cтраница 3
 |
Химический состав исходных минералов. [31] |
Осаждение в условиях перемешивания при высокой концентрации ванадия в растворе лимитируется диффузией вещества из объема раствора и поверхности растущих частиц, а в конце осаждения - реакцией первого порядка на поверхности частиц. [32]
В; Я - глубина погружения цилиндра в ванну, см; р - удельное объемное электрическое сопротивление лакокрасочного материала в ванне, Ом - см; i - плотность тока в конце осаждения. [33]
Химизм взаимодействия в системе Cu ( NOs) a - NaOH-НЮ резко усложняется, если осаждение вести при прямой подаче осадителя ( ОН - Си2), так как возникает иная химическая среда, в которой происходит реакция, а именно, [ вместо избытка ОН существует избыток Си2 1 в суспензии, который постепенно уменьшается к концу осаждения. В этом случае наряду с реакцией (8.1) первичного образования осадка протекают вторичные гетерогенные химические реакции. [34]
Раствор, содержащий 0 2 - 5 мг Ni, подогревают до начала кипения, прибавляют раствор ацетата натрия или аммиака до щелочной реакции по метиловому красному, приливают постепенно раствор а-бензилдиоксима в ацетоне до полноты образования осадка, добавляют 10 - 20 мл ацетона ( в зависимости от количества никеля), следя, чтобы к концу осаждения фильтрат был окрашен в желтый цвет. Затем осадок отфильтровывают, промывают горячей водой, сушат до постоянного веса при 120 - 130 С и взвешивают. [35]
Ьн с содержимым помещают в ванну с холодной водой, прибавляют для окисления ванадия по каплям перманганат до слаборозовой окраски и затем осаждают титан и ванадий 30 мл раствора купферрона ( 60 г / л), прибавляя его по каплям при пог стоянием перемешивании стеклянной палочкой до появления белого - осадка, пе исчезающего при перемешивании и указывающего на конец осаждения титана. [36]
Это можно сделать, если известны качественный состав анализируемого раствора и электрохимические характеристики присутствующих в нем ионов. Конец осаждения каждого из них устанавливают по резкому падению силы тока. Электрическую энергию, необходимую для проведения электроанализа при постоянной силе тока и при постоянном потенциале электрода, получают от какого-либо внешнего источника постоянного тока. [37]
Метод Фольгарда как более удобный распространен значительно больше, чем метод Мора. Конец осаждения при этом методе определяют при помощи индикатора. В качестве индикатора Фольгард рекомендует железо-аммонийные квасцы NH4Fe ( SO4) 2 12 Н2О, которые в виде насыщенного раствора должны прибавляться к титруемой жидкости всегда в определенном количестве. Применение этой соли в качестве индикатора основано на следующем. [38]
Например, при осаждении сульфата бария прибавляют НС1, которая повышает растворимость его вследствие образования Н5О4 - ионов. К концу осаждения эту повышенную растворимость BaS04 снова понижают прибавлением умеренного избытка оса-дителя. [39]
В начале осаждения растворимость рекомендуют повышать также подкислением раствора. К концу осаждения растворимость вновь уменьшают. Например, СаС2О4 вначале осаждают из кислого раствора, чтобы получить более крупные кристаллы; в конце для полного осаждения добавляют по каплям аммиак, нейтрализующий избыток кислоты. Нагревание способствует получению более плотных и легко отфильтровываемых осадков. [40]
В начале осаждения растворимость рекомендуют повышать также подкислением раствора. К концу осаждения растворимость должна быть вновь уменьшена. Например, осаждение СаС2О4 вначале ведут из кислого раствора, чтобы получить более крупные кристаллы, в конце для полного осаждения добавляют по каплям-аммиак, нейтрализующий избыток кислоты. Нагревание способствует получению более плотных и легко фильтруемых осадков. После осаждения кристаллический осадок рекомендуется оставить стоять в маточном растворе от 1 до 12 ч для созревания, представляющего собой процесс рекристаллизации частиц осадка. При рекристаллизации происходит упорядочение расположения отдельных, ионов в кристаллической решетке, укрупнение первичных частиц осадка, что связано с большей растворимостью мелких частиц осадка. При рекристаллизации частично освобождаются посторонние ионы, захваченные осадком во время и после осаждения. [41]
 |
Отмывка окиси серебра. [42] |
Раствор щелочи по каплям добавляют к энергично перемешиваемому раствору нитрата серебра. В конце осаждения необходим небольшой избыток серебра. Осадок следует 30 - 40 раз промыть дистиллированной водой. Для этой операции удобен цилиндр с притертой пробкой, в котором окись энергично встряхивается с водой. Эти данные получены Бейтсом и Бауэром при получении окиси серебра. Постоянство электропроводности, которое показывает, что растворимые электролиты отмыты, наступает после того, как окись была промыта не менее 25 раз. [43]
Вторым видом соосаждения является адсорбция примесей. В конце осаждения в этом случае в растворе будет находиться некоторый избыток ионов бария, а содержание сульфат-ионов будет исчезающе мало. Установлено, что осаждение не обязательно заканчивается переходом на поверхность кристаллов ионов осаждающегося вещества в строго стехиометрическом соотношении. В ряде узлов кристаллической решетки сульфата бария на поверхности кристаллов будет находиться некоторый избыток против стехиомет-рического содержания тех ионов кристаллической решетки, которые находятся в избытке в растворе. [44]
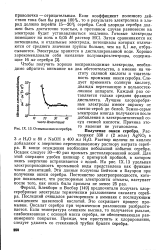 |
Отмывка окиси серебра. [45] |
Страницы: 1 2 3 4