Диаграмма - оргел
Cтраница 4
Такое построение называется диаграммой Оргела. Сравнение с рис. 12.12 показывает, что тетраэдрическая - диаграмма, по существу, тождественна октаэдрической диаграмме ds ( положительная дырка d2), так что диаграмма Оргела содержит информацию, относящуюся к dn - и - конфигурациям октаэдрических и тетраэдрических комплексов. [46]
Электронные спектры комплексов кобальта ( П) во многих случаях могут дать ценную структурную информацию. Большинство шести-координационных комплексов имеют высокоспиновую электронную конфигурацию. Диаграмма Оргела этих комплексов представлена на рис. 10.11. Основное их состояние - 4Т 9, и спин-орбитальное взаимодействие значительно. Переход 4Tlg ( F) - 4A2g двухэлектронный и не неблюдается. Плечо появляется потому, что спин-орбитальное взаимодействие в возбужденном состоянии 4Т19 ( Р) снимает вырождение. [47]
 |
Частичная диаграмма Танабе-Сугано для конфигурации d5. [ IMAGE ] Частичная диаграмма Танабе-Сугано для конфигурации d1. [48] |
Так, при обсуждении конфигурации d2 ( V3) мы интересовались только триплет-триплетными переходами, поэтому был необходим только параметр Рака В. Если в диаграмму включаются синглет-ные уровни, необходим параметр Рака С и должно быть определено отношение С / В. Соответственно, когда имеется пересечение зависимостей Е от АО ( на диаграмме Оргела), на Т - S-диаграмме будет наблюдаться излом зависимостей Е / В от Д0АВ, так как в точке пересечения ось х соответствует различным уровням. [49]
Если же использовать уточненные значения В и С, то получатся достаточно точные диаграммы энергетических уровней. Однако из-за их многочисленности это слишком неудобно для повседневного использования: необходимы более наглядные диаграммы, включающие учет влияния переменной силы поля лигандов. На рис. 10.54 и 10.55 показаны более сложные ( и более информативные) диаграммы Оргела. Термы одной и той же симметрии ( в данном случае Т е) не могут пересекаться, поскольку чем ближе они подходят друг к другу, тем больше будет их смешивание, приводящее к повышению энергии более высокого уровня и понижению энергии более низкого уровня. Смешивание Груровней больше в тетраэдрическом поле, чем в октаэдрическом, поскольку по мере возрастания силы поля термы F и Р в первом случае сближаются, а во втором - удаляются. [50]
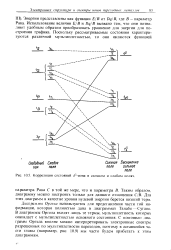 |
Корреляция состояний / 2-иона в сильном и слабом полях. [51] |
Для этих диаграмм в качестве уровня нулевой энергии берется низший терм. Диаграммы Оргела используются для представления части той информации, которая полностью дана в диаграммах Танабе - Сугано. В диаграммы Оргела входят лишь те термы, мультиплетность которых совпадает с мультиплетностью основного состояния. С помощью диаграмм Оргела вполне можно интерпретировать электронные спектры разрешенных по мультиплетности переходов, поэтому в оставшейся части главы ( например, рис. 10.9) мы часто будем прибегать к этим диаграммам. [52]
Для этих диаграмм в качестве уровня нулевой энергии берется низший терм. Диаграммы Оргела используются для представления части той информации, которая полностью дана в диаграммах Танабе - Сугано. В диаграммы Оргела входят лишь те термы, мультиплетность которых совпадает с мультиплетностью основного состояния. С помощью диаграмм Оргела вполне можно интерпретировать электронные спектры разрешенных по мультиплетности переходов, поэтому в оставшейся части главы ( например, рис. 10.9) мы часто будем прибегать к этим диаграммам. [53]
Для этих диаграмм в качестве уровня нулевой энергии берется низший терм. Диаграммы Оргела используются для представления части той информации, которая полностью дана в диаграммах Танабе - Сугано. В диаграммы Оргела входят лишь те термы, мультиплетность которых совпадает с мультиплетностью основного состояния. С помощью диаграмм Оргела вполне можно интерпретировать электронные спектры разрешенных по мультиплетности переходов, поэтому в оставшейся части главы ( например, рис. 10.9) мы часто будем прибегать к этим диаграммам. [54]
Если, как предсказывает теория кристаллического поля, имеет место расщепление d - орбита-лей на два новых уровня - трижды вырожденный de и дважды вырожденный dy, то можно предположить, что поглощение является результатом возбуждения единственного электрона с de - на dy - уровень. Принимая, что разность в энергиях между основным и возбужденным уровнями равна IQDq, находим, что Dq 20400слг1 / 10 2040cjn - 1 для воды как лиганда. Эта последовательность показывает увеличение силы поля лиганда в ряду Н2О NH3 ЭДА. В системах с числом d - электронов, меньшим 9, свободный ион из-за внутриэлектронного отталкивания характеризуется целым набором термов, которые усложняют картину. Кроме того, необходимо установить, как каждый из этих термов расщепляется далее под влиянием различных полей лигандов. Для этого рассмотрим только кубическое возмущающее поле. Можно построить диаграмму, называемую диаграммой Оргела, которая показывает, как расщепляются атомные термы под действием кристаллического поля, увеличивающегося по интенсивности. Расчет расщепления требует квантовомеханического вычисления возмущений с использованием приближенных невозмущенных волновых функций и приближенных величин для возмущающих полей. По этой причине вычисления всегда приближенные. [55]
Если, как предсказывает теория кристаллического поля, имеет место расщепление d - орбита-лей на два новых уровня - трижды вырожденный de и дважды вырожденный dy, то можно предположить, что поглощение является результатом возбуждения единственного электрона с ds - на с ( у-уровень. Принимая, что разность в энергиях между основным и возбужденным уровнями равна lODq, находим, что Dq 20 400см - 1 / 10 2040см 1 для воды как лиганда. Эта последовательность показывает увеличение силы поля лиганда в ряду Н2О NH3 ЭДА. В системах с числом d - электронов, меньшим 9, свободный ион из-за внутриэлектронного отталкивания характеризуется целым набором термов, которые усложняют картину. Кроме того, необходимо установить, как каждый из этих термов расщепляется далее под влиянием различных полей лигандов. Для этого рассмотрим только кубическое возмущающее поле. Можно построить диаграмму, называемую диаграммой Оргела, которая показывает, как расщепляются атомные термы под действием кристаллического поля, увеличивающегося по интенсивности. Расчет расщепления требует квантовомеханического вычисления возмущений с использованием приближенных невозмущенных волновых функций и приближенных величин для возмущающих полей. По этой причине вычисления всегда приближенные. [56]
Если, как предсказывает теория кристаллического поля, имеет место расщепление d - орбита-лей на два новых уровня - трижды вырожденный de и дважды вырожденный dy, то можно предположить, что поглощение является результатом возбуждения единственного электрона с ds - на - уровень. Принимая, что разность в энергиях между основным и возбужденным уровнями равна ODq, находим, что Dq 20 400сж - 1 / 10 204 0 слг1 для воды как лиганда. Каждый из этих уровней, в частности возбужденный Eg уровень, в тетрагональном поле расщепляется дальше, например, вследствие искажения, вызванного эффектом Яна - Теллера. Эта последовательность показывает увеличение силы поля лиганда в ряду Н2О NH3 ЭДА. В системах с числом d - электронов, меньшим 9, свободный ион из-за внутриэлектронного отталкивания характеризуется целым набором термов, которые усложняют картину. Кроме того, необходимо установить, как каждый из этих термов расщепляется далее под влиянием различных полей лигандов. Для этого рассмотрим только кубическое возмущающее поле. Можно построить диаграмму, называемую диаграммой Оргела, которая показывает, как расщепляются атомные термы под действием кристаллического поля, увеличивающегося по интенсивности. Расчет расщепления требует квантовомеханического вычисления возмущений с использованием приближенных невозмущенных волновых функций и приближенных величин для возмущающих полей. По этой причине вычисления всегда приближенные. [57]
 |
Диаграмма Оргела. [58] |
Последний ряд называется спектрохимическим, так как он получен из Данных спектров поглощения комплексов в видимой и ультрафиолетовой областях. Лиганды, стоящие в конце такого ряда, оказывают большое воздействие на центральный ион, приводя к значительному расщеплению. Их называют лигандами сильного поля. Лиганды слабого поля расположены в начале спектрохимического ряда. Когда центральный ион имеет более одного cf - электрона, кабина расщепления его состояний заметно усложняется. При этом существенную роль играет межэлектронное взаимодействие. Однако, согласно правилу дополнительности, электронную конфигурацию, содержащую п d - электронов, можно представить как 10 - п электронных дырок в замкнутой с ( 10-оболочке, что значительно упрощает рассмотрение многоэлектронных состояний. Поведение таких электронных дырок аналогично поведению электронов с той лишь разницей, что дырку следует считать положительно заряженной. Конфигурации dn и d10 - n в этом случае имеют взаимно перевернутые схемы расщепления состояний. На рис. 6.9 показано соотношение между октаэдрическими и тетраэдрическими расщеплениями для некоторых электронных конфигураций. Подобные диаграммы называются диаграммами Оргела. В других случаях диаграммы Оргела имеют более сложный вид. [59]
Последний ряд называется спектрохимическим, так как он получен из Данных спектров поглощения комплексов в видимой и ультрафиолетовой областях. Лиганды, стоящие в конце такого ряда, оказывают большое воздействие на центральный ион, приводя к значительному расщеплению. Их называют лигандами сильного поля. Лиганды слабого поля расположены в начале спектрохимического ряда. Когда центральный ион имеет более одного cf - электрона, кабина расщепления его состояний заметно усложняется. При этом существенную роль играет межэлектронное взаимодействие. Однако, согласно правилу дополнительности, электронную конфигурацию, содержащую п d - электронов, можно представить как 10 - п электронных дырок в замкнутой с ( 10-оболочке, что значительно упрощает рассмотрение многоэлектронных состояний. Поведение таких электронных дырок аналогично поведению электронов с той лишь разницей, что дырку следует считать положительно заряженной. Конфигурации dn и d10 - n в этом случае имеют взаимно перевернутые схемы расщепления состояний. На рис. 6.9 показано соотношение между октаэдрическими и тетраэдрическими расщеплениями для некоторых электронных конфигураций. Подобные диаграммы называются диаграммами Оргела. В других случаях диаграммы Оргела имеют более сложный вид. [60]
Страницы: 1 2 3 4