Константа - диссоциация - слабая кислота
Cтраница 2
Величины констант диссоциации слабых кислот и щелочей были определены Оствальдом и другими исследователями еще в конце прошлого века. Определение было основано на интерпретации данных о нелинейном возрастании электропроводности слабых электролитов при их разбавлении. Хотя этот метод был впоследствии теоретически и экспериментально усовершенствован и его точность доведена до очень высокого уровня, сейчас он не находит широкого применения, и поэтому в этой книге рассматриваться не будет. [16]
Значение константы диссоциации слабой кислоты характеризует равновесие процесса диссоциации независимо от концентрации кислоты в растворе. При заданной общей концентрации кислоты процесс диссоциации можно охарактеризовать по степени диссоциации, которая представляет собой отношение числа ( или концентрации) диссоциированных молекул к общему числу ( или концентрации) молекул кислоты в растворе. Степень диссоциации, конечно, зависит от концентрации. [17]
Зная константу диссоциации слабой кислоты ( или основания), легко вычислить концентрацию ионов водорода ( или гид-роксила), применяя закон разбавления Оствальда. [18]
Зная константу диссоциации слабой кислоты ( или основания), легко вычислить концентрацию ионов водорода ( гидроксила) в ее растворе. [19]
Зная константу диссоциации слабой кислоты ( или основания)), легко вычислить концентрацию ионов водорода ( гидроксила) в ее растворе. [20]
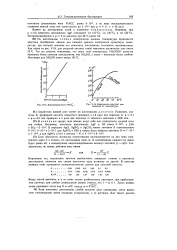 |
Диссоциация иона TINO I.| Зависимость констант диссоциации от температуры. [21] |
Зная константу диссоциации слабой кислоты ( или основания), легко вычислить концентрацию ионов водорода ( гидроксила) в ее растворе. [22]
Зная константу диссоциации соответствующей слабой кислоты или основания, нетрудно вычислить рН образуемых ими буферных смесей. Выведем формулы, применяемые при указанных вычислениях. [23]
При этом константа диссоциации слабой кислоты берется по второй ступени, так как в результате гидролиза получаются анионы НСО3 -, образующиеся из СО3 - - и Н - ионов воды. [24]
Ниже приведены константы диссоциации слабых кислот и коэффициенты п, характеризующие увеличение растворимости в одномолярном растворе сильной кислоты. [25]
Требуется знать константы диссоциации слабой кислоты, титруемой сильным основанием ( 1), или слабого основания, титруемого сильной кислотой ( 2), а также концентрацию образующей соли. [26]
К кисл - константа диссоциации соответствующей слабой кислоты. Оно справедливо для всех солей, образованных слабыми кислотами и сильными основаниями. [27]
Результаты титрования позволяют определять константы диссоциации слабых кислот и оснований, в том числе полифункциональных. По этой причине потенциометрический метод является одним из важнейших методов изучения полиэлектролитов, в том числе и биополимеров, таких как белки, полипептиды, нуклеиновые кислоты. [28]
Целью задачи является определение константы диссоциации слабой кислоты и константы гидролиза ее соли. [29]
Найденные различными способами значения констант диссоциации слабых кислот приведены в табл. II. [30]
Страницы: 1 2 3 4