Константа - диссоциация - слабая кислота
Cтраница 3
Целью задачи является определение константы диссоциации слабой кислоты и константы гидролиза ее соли и сильным основанием. [31]
Количественно исследуя зависимость между константами диссоциации слабых кислот и оснований и их каталитическим действием в реакции с глюкозой, Бренстед описал кинетическое действие соли, как эффект, наложенный на главный каталитический эффект в кислотном катализе или в катализе основаниями. Бренстед считал, что солевой эффект вызывается изменениями среды, в которой происходит реакция, и связан линейной зависимостью с концентрацией. [32]
Показатель рКкисл - отрицательный логарифм константы диссоциации слабой кислоты - называется силовым показателем кислоты. [33]
Рассмотренные вычисления иллюстрируют значение величин констант диссоциации слабой кислоты, соль которой мы осаждаем. Эти вычисления показывают также, что приемлемый результат часто можно получить сравнительно простым способом, именно, пренебрегая образованием недиссоциированных молекул слабой кислоты. Однако такое упрощение допустимо не всегда. Как поступать в тех случях, когда оно недопустимо, показывают следующие примеры. [34]
Рассмотренные вычисления иллюстрируют значение величин констант диссоциации слабой кислоты, соль которой мы осаждаем. Эти вычисления показывают также, что приемлемый результат часто можно получить сравнительно простым способом, именно, пренебрегая образованием недиссоциированных молекул слабой кислоты. Однако такое упрощение допустимо не всегда. Как поступать в тех случаях, когда оно недопустимо, показывают следующие примеры. [35]
Вполне понятно, что чем меньше константа диссоциации слабой кислоты и чем больше концентрация сильной, тем более точным будет определение сильной кислоты. [36]
Предложите способ ( ы) определения константы диссоциации слабой кислоты, если известна константа диссоциации, другой слабой кислоты. [37]
Следовательно, константа гидролиза обратно пропорциональна константе диссоциации слабой кислоты: чем слабее кислота, тем больше константа гидролиза ее соли. [38]
Выражение ( 5 - 34) для константы диссоциации слабой кислоты получено при помощи двух уравнений, основанных на законах сохранения. Это уравнение материального баланса, согласно которому общее количество аниона кислоты в растворе остается постоянным, а также уравнение баланса зарядов, согласно которому раствор в целом должен оставаться нейтральным. Выражение для константы диссоциации слабой кислоты может рассматриваться как квадратное уравнение, которое решают прямым путем или методом последовательных приближений; оно справедливо для растворов, кислотность которых достаточно высока, чтобы можно было пренебречь вкладом в [ Н ] самодиссоциации воды. Кислотно-основные индикаторы сами являются слабыми кислотами или слабыми основаниями, обладающими различной окраской в диссоциированной и недиссоциированной формах. [39]
Степень гидролиза обратно пропорциональна корню квадратному из константы диссоциации слабой кислоты. [40]
Это первая и простейшая форма выражения для константы диссоциации слабой кислоты, которая использовалась нами в разд. [41]
Степень гидролиза обратно пропорциональна корню квадратному из константы диссоциации слабой кислоты. [42]
Степень гидролиза зависит в первую очередь от константы диссоциации слабой кислоты, образующей соль. Например, цианид натрия NaCN образован слабой синильной кислотой HCN. [43]
Таким образом, буферная сила зависит от констант диссоциации слабых кислот или оснований стандартного и испытуемого растворов. [44]
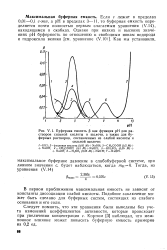 |
Буферная емкость р как функция рН для ра. [45] |
Страницы: 1 2 3 4