Константа - комплексообразование
Cтраница 1
Константы комплексообразования этих циклических соединений значительно выше ( в 63 - 1 99 106 раза), чем у линейных р-дикетонов. [1]
Константы комплексообразования для обеих фаз различны, что, однако, не имеет значения для последующих рассуждений. [2]
Константы комплексообразования ( константы устойчивости, диссоциации, общие, индивидуальные) 11 ел. [3]
Константа комплексообразования для - равна 790; растворимость Ь ( тв. [4]
Константы комплексообразования этих циклических соединений значительно выше ( в 63 - 1 99 106 раза), чем у линейных р-дикетонов. [5]
Константы комплексообразования катионов с циклическим эфиром, имеющим подходящую по размеру внутреннюю полость, обычно очень высоки, поэтому соответствующие комплексы образуются практически с количественным выходом. Так, добавка дициклогексано-18 - краун-6 к бензолу приводит к растворимости в нем эквимольных количеств КМпО4 или КС1, совершенно нерастворимых в чистом бензоле. Растворенные в малополярных растворителях соли с закомплексованными или объемистыми органическими катионами имеют высокую нуклеофиль-ную и каталитическую активность. [6]
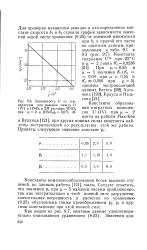 |
Зависимость k от температуры для реакции между U ( IV и HNO2 в 2М растворе HNO3 при ц 2 я [ HNO2 ] 0 0 075 М. [7] |
Константы комплексообразования более высоких ступеней, по данным работы [121], малы. Следует отметить, что значения р при ц 5 найдены весьма приближенно, так как экстраполяция к этой ионной силе затруднена; значительная погрешность в расчетах по уравнению (9.25) обусловлена также пренебрежением р3, и и другими константами при этой ионной силе. [8]
Измерены константы комплексообразования ( константы устойчивости) для ряда комбинаций краун-эфир - неорганическая соль - растворитель посредством УФ-спектроскопии, калориметрии, с помошью ионоселективных электродов и другими способами. Получены данные по термодинамике, а недавно стало возможным с помошью ЯМР-спектроско-пии на ядрах Н, 7Li, Na, 39K и 133Cs измерить и кинетические параметры, такие, как константы комплексообразования или константы диссоциации. Как отмечалось ранее, комплексы краун-эфиров с катионами становятся растворимыми даже в неполярных органических растворителях благодаря гидрофобной природе органических фрагментов, расположенных по внешней стороне полиэфирного кольца. [9]
Определить константы комплексообразования сор-батов с производным фосфолена. [10]
Расчет констант комплексообразования косвенным методом оказывается более простым, чем. [11]
Большинство констант комплексообразования, приведенных в табл. 2, было измерено посредством регистрации изменений экстрагируемости комплекса тория с ТТА бензолом при введении в водную фазу различных анионов. Поэтому литература, указанная в табл. 2, может быть использована для получения более определенной информации об экстракции тория в присутствии комплексообразующих ионов. [12]
Расчеты константы комплексообразования Кс, по Гхошу и Миттеру, могут дать правильную картину относительной прочности комплексов с различными кислотами лишь тогда, когда измерения проводят в области приблизительно полной диссоциации. [13]
Для определения констант комплексообразования и коэффициентов распределения был применен ионообменный метод. Особенно существенным с точки зрения хроматографии является знание величины константы равновесия распада комплексного иона под действием ионов водорода. [14]
Приводимые значения констант комплексообразования термодинамически не являются вполне строгими, так как при их расчете использовались не активности, а концентрации ионов. [15]
Страницы: 1 2 3 4 5