Константа - комплексообразование
Cтраница 3
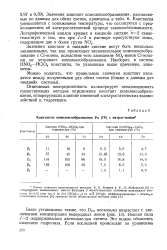 |
Константы комплексообразования Ри ( IV с нитрат-ионом. [31] |
Отмечаемая неопределенность иллюстрирует неполноценность существующих методов определения констант комплексообразования, игнорирующих влияние изменений электростатических взаимодействий и гидратации. [32]
 |
Зависимость оптической плотности от состава мономерной смеси.| График для определения константы комплексообразования. [33] |
Написать структуру комплекса и оценить по значению константы комплексообразования к какому типу относится данный комплекс. [34]
Коэффициент распределения является функцией константы обмена и констант комплексообразования элемента. [35]
В системах, где лигандами являются анионы, константы комплексообразования низших катионных и нейтральных комплексов могут быть определены различными способами. Значительно сложнее определить константы для высших анионных комплексов, часто трудно бывает даже доказать их существование. [36]
Если применимо уравнение (2.17), то можно рассчитать константу комплексообразования К. [37]
Таким образом, коэффициент разделения двух элементов определяется константами комплексообразования их с экстрагентом и с анионами в водном растворе, а также концентрацией экстрагента в органической фазе. Сопоставляя эти константы для скандия с одноименными величинами для тория и циркония ( табл. 4), видим, что наиболее благоприятной средой для разделения скандия и тория являются азотнокислые растворы, а для разделения пары скандий-цирконий - солянокислые растворы. С целью увеличения коэффициента разделения элементов необходимо, чтобы в процессе экстракции сохранялась высокая концентрация анионов в водном растворе. [38]
В реакции комцлексообразования константа устойчивости ( известная также как константа комплексообразования), которая является константой равновесия реакции и обратно пропорциональна константе диссоциации, показывает степень комплексообразования и устойчивость полученного комплекса в растворе. С точки зрения термодинамики константа устойчивости может быть представлена как мера тедлотворной способности и изменения энтропии реакции комцлексообразования, потому что устойчивость образуемого комплекса увеличивается с повышением теплотворной способности и энтропии реакции. [39]
В реакции комплексообразования константа устойчивости ( известная также как константа комплексообразования), которая является константой равновесия реакции и обратно пропорциональна константе диссоциации, показывает степень комплексообразования и устойчивость полученного комплекса в растворе. С точки зрения термодинамики константа устойчивости может быть представлена как мера тедлотворной способности и изменения энтропии реакции комплексообразования, потому что устойчивость образуемого комплекса увеличивается с повышением теплотворной способности и энтропии реакции. [40]
 |
Кривые сила тока - напряжение Cd2 с нитрилуксусной кислотой, полученные с помощью ртутного. [41] |
Однако по этой формуле не удается получить постоянного значения константы комплексообразования. Кроме того, оказывается, что высота первой ступени не пропорциональна ( в соответствии с уравнением Ильковича) корню квадратному из скорости вытекания ртути. [42]
В качестве третьего условия здесь прибавляется следующее: величины констант комплексообразования должны быть такими, чтобы дифференциальную кривую поглощения можно было разбить на интервалы, в каждом из которых концентрацией одного или нескольких комплексов можно пренебречь. Тогда каждая из полученных кривых может быть приписана только одному комплексному иону. [43]
Оно, очевидно, равно необходимо при хроматографи-ческом определении любых констант комплексообразования. [44]
Соотношение ( 111 - 56) дает возможность найти величину константы комплексообразования по одним лишь относительным величинам удерживаний в жидкостях В и S, разумеется, при одной температуре. Тем не менее оценки величин AI и соответственно энтропии А5 представляются менее надежными, чем оценки ДЯ. [45]
Страницы: 1 2 3 4 5