Константа - равновесие
Cтраница 2
Константа равновесия для любых окислительно-восстановительных процессов может быть вычислена, если известны окислительно-восстановительные потенциалы пар, соответствующие взятым окислителю и восстановителю. [16]
Константа равновесия может быть определена измерением концентраций в равновесном состоянии. Кроме того, справочные данные по величинам ДО0 реакций образования для большого числа веществ во многих случаях позволяют рассчитать по ним AG интересующей реакции и, следовательно, константу равновесия, не производя эксперимента. [17]
Константа равновесия К может быть также представлена в виде соотношения функций распределения. [18]
Константы равновесия для молекулярных реакций при 900 К были получены на основании данных Национального бюро стандартов США; константы равновесия для сво-боднорадикальиых реакций получены экстраполированием данных к 300 К. [19]
Константа равновесия при 100 ЛГравн 6 2 - 103 атм-1. Вычислить изменение энтропии в реакции, д) Опытным путем установлено, что скорость реакции нулевого порядка по концентрации В. [20]
Константа равновесия, подобная (12.2), может быть записана также и для других сопряженных кислотно-основных систем. [21]
Константа равновесия определяется константами диссоциации как индикатора, так и кислоты и может быть вычислена из констант ионизации кислоты и индикатора. [22]
Константа равновесия / С в таких случаях называется константой электролитической диссоциации. [23]
Константа равновесия этой реакции такова, что окисление ионов S - - происходит уже при столь малых концентрациях их в растворе, при которых связывание ионами Н не может иметь места. Следовательно, причиной наблюдаемого различия в действии НС1 и НМОз на сульфиды IV группы является тоже различие в величинах констант равновесия тех реакций, благодаря течению которых происходит удаление ионов S - - из раствора. [24]
 |
Накопление ( 1 и расходование ( 2 йодистого водорода. [25] |
Константа равновесия зависит от температуры по экспоненциальному закону. Вант-Гофф впервые обратил внимание на то, что из этого следует экспоненциальная зависимость от температуры такжо и констант скорости реакций. [26]
Константа равновесия (4.21) была измерена [886], и тем самым была определена основность в широком интервале с учетом коэффициентов активности в ионной среде. Данные по алкил-замещенным ароматическим углеводородам [869, 887] ( табл. 4.6) и по незамещенным конденсированным ароматическим углеводородам [886] ( табл. 4.13) были получены именно таким путем. Корреляция этих данных с данными тю измерению электропроводности [783] ( табл. 4.6) не оставляет сомнения в том, что взаимодействие, обеспечивающее экстракцию углеводородов в кислую фазу, приводит к образованию ионов. [27]
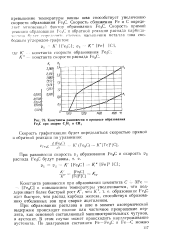 |
Константы равновесия в процессе образования Fe3C при сварке. и СН4. [28] |
Константа равновесия при образовании цементита С - г 3Fe - [ Fe3C ] с повышением температуры увеличивается, что поддерживает более быстрый рост К. [29]
Константы равновесия определяют экспериментально, так как при большом числе компонентов расчеты их весьма сложны. Однако обычно можно ограничиться учетом основных компонентов нефти в данной залежи и, зная давление и температуру, установить расчетным путем, в каком фазовом состоянии находится смесь, а на основе этого сделать выводы об относительной высоте газовой шапки и предсказать изменение фазового состояния нефти при уменьшении давления и температуры в процессе эксплуатации залежи. [30]
Страницы: 1 2 3 4