Константа - равновесие - данная реакция
Cтраница 1
Константа равновесия данной реакции зависит от температуры и давления, но не зависит от концентрации реагирующих веществ. Присутствие катализатора также не влияет на константу равновесия; он одновременно увеличивает скорость прямой и обратной реакций, а поэтому только уменьшает время достижения равновесия. [1]
Определить константу равновесия данной реакции и исходные концентрации кислоты и спирта, если в момент равновесия в реакционной смеси содержится по V8 моль кислоты и спирта и по 2 / 3 моль эфира и воды. [2]
Определить константу равновесия данной реакции и исходные концентрации кислоты и спирта, если в момент равновесия в реакционной смеси содержится по 1 / 3 моль кислоты и спирта и по 2 / 3 моль эфира и воды. [3]
Определить константу равновесия данной реакции и исходные концентрации кислоты и спирта, если в момент равновесия в реакционной смеси содержится по / з моль кислоты и спирта и по 2 / з моль эфира и воды. [4]
Вычислим константу равновесия данной реакции при t 600 С. [5]
 |
Равновесные массовые доли аммиака. [6] |
Проведем расчет константы равновесия данной реакции при повышенном давлении ( 30 МПа), приняв, что реакционная смесь является идеальным раствором реальных газов. [7]
Численное значение константы равновесия данной реакции определяет ее выход. Выходом реакции называют отношение количества получаемого в действительности продукта к тому количеству, которое получилось бы при протекании реакции до конца. [8]
Величина К представляет константу равновесия данной реакции и равняется отношению произведения равновесных концентраций веществ, получившихся в результате реакции, к произведению равновесных концентраций веществ, вступающих в реакцию. [9]
Специфические ошибки определяются величиной константы равновесия данной реакции и точностью обнаружения точки эквивалентности. Специфические ошибки и являются ошибками титрования. Они не зависят от точности экспериментальной работы, так как порождаются особенностями применяемой химической реакции и химической природой индикатора. [10]
Какой вид имеет выражение для константы равновесия Кр данной реакции. [11]
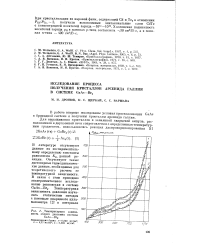 |
Температурная зависимость общего давления системы GaAs - Вг2. [12] |
В литературе отсутствуют данные по экспериментальному определению константы равновесия Kft данной реакции. Отсутствуют также достоверные термодинамические данные, необходимые для теоретического расчета ее температурной зависимости. [13]
Следовательно, для нахождения величины L необходимо знать константу равновесия данной реакции. [14]
Таким образом, для нахождения величины А необходимо знать константу равновесия данной реакции. [15]
Страницы: 1 2 3