Константа - связывание
Cтраница 1
Константы связывания ГФЛ, ациламинокислот и ингибиторов, содержащих карбоксильные группы, существенно изменяются при удалении цинка. [1]
 |
Элюирование - нитрофенола на. [2] |
Определение констант связывания К и констант ингибирования / Ci для мицеллярно-каталитических реакций позволяет, по крайней мере качественно, интерпретировать влияние структуры субстрата на природу процесса комплексообразования с мицеллами и дает возможность сравнить константы связывания в мицеллярных системах с константами связывания в ферментативных реакциях. Ограниченное число данных такого рода не позволяет пока сделать каких бы то ни было широких обобщений. [3]
Индексация констант связывания К ( х, ji) или К ( у, / а) указывает на взаимодействие с ферментом субстрата со степенью полимеризации х или у так, что восстанавливающий конец субстрата приходит в контакт с сайтом / 4 или / 2 соответственно. [4]
 |
Экспериментальные данные для реакции FlAKNa - ПДМАЭМ, представленные в координатах уравнения. [5] |
Определяя константы связывания звеньев полиэлектролитов в ионные пары / С2 хар и / С 2, хар, а также функцию кооперативное реакции ф ( 0) и ср ( 9) для конкретных систем, можно сопоставлять эти системы по эффективности кооперативного взаимодействия. [6]
Достаточно часто константу связывания До и концентрацию активных центров связывания - определяют с помощью метода двойных обратных величин. [7]
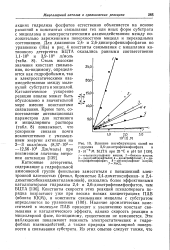 |
Влияние ингибирующих солей на гидролиз 2 6-динитрофенилфосфата в 3 - 10 - 3М БЦТА при 25 С и рН 9 0. [8] |
Столь высокие значения констант связывания, по-видимому, определяются как гидрофобными, так и электростатическими взаимодействиями между молекулой субстрата и мицеллой. Каталитическое ускорение реакции вполне может быть обусловлено в значительной мере именно константами связывания. [9]
Следует отметить, что константы связывания для обоих сложных эфиров мало отличаются. Об образовании комплекса можно судить на том основании, что скорость реакции стремится к пределу как при увеличении концентрации субстрата, так и декстрина. Интересно сравнить скорости ацилирования, протекающего внутри такого комплекса, с бимолекулярной реакцией ацилирования соответствующего сахара в растворе. [10]
Величины каталитических эффектов и констант связывания в этих системах, а также важность гидрофобных взаимодействий свидетельствуют о возможности использования таких функциональных агрегатов как моделей для изучения ферментативного катализа и структуры белков. [11]
В общем случае зависимость константы связывания ионного реагента от концентрации ПАВ может быть определена в независимом эксперименте. Например, в работе [16] для этой цепи была использована зависимость кажущейся величины рКа ионного реагента ( бензимидазола) от концентрации ЦТАБ. Зависимость рассчитанной таким образом аффективной величины константы связывания анионного реагента ( КА -) от концентрации ПАВ показана на рис. 13.3 В. [12]
Такое рассмотрение предполагает, что константы связывания различны. [13]
Если непродуктивное связывание преобладает, константа продуктивного связывания будет так мала, что не будет давать заметного вклада в наблюдаемую константу связывания. [14]
После того как была обнаружена идентичность констант связывания металла с двумя центрами белка, тотчас же возник вопрос, идентичны ли сами связывающие центры. Эту проблему особенно трудно решить для белков, построенных из одной полипептидной цепи. И физиологические, и физические исследования пролили свет на эту еще не до конца решенную проблему, к которой мы ниже вернемся. [15]
Страницы: 1 2 3 4