Константа - скорость - реакция - окисление
Cтраница 2
В более ранних исследованиях5 было установлено, что константы скорости реакции окисления сернистого ангидрида на ванадиевых катализаторах выражаются графически двумя прямыми, пересекающимися примерно при 450 С. [16]
Существование такой зависимости позволяет утверждать, что величины констант скоростей реакций окисления R2NO определяются в основном теми же факторами, что и константы скоростей реакций внешнесферного окисления таких доноров, как ионы металлов и их комплексы, неорганические анионы. [17]
Из уравнения ( VI1 - 18) следует, что константа скорости реакции окисления является множителем в левой части этой формулы. Следовательно, время окисления NO до заданной степени обратно пропорционально константе скорости, которая зависит только от температуры. [18]
Константы скорости обмена СО 2 и восстановления поверхности почти равны, а константы скорости реакции окисления СО на порядок больше. Данные кинетического и изотопного анализа показывают невозможность сведения реакции окисления окиси углерода на Мп02 к попеременному восстановлению-окислению поверхности. [19]
Эксперименты по термокаталитической очистке отходящих газов от паров метилметакрилата на оксидном железохромовом катализаторе позволили рассчитать значение константы скорости реакции окисления метилметакрилата k для ряда температур t ( С) ( табл. 2.5) [7], зависимость k f ( t) ( рис. 2.3) имеет вид достаточно характерный, похожий на экспоненциальную зависимость. [20]
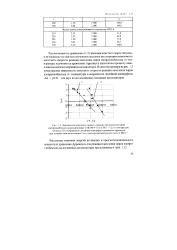 |
Зависимость константы скорости реакции ( k окисления паров изопропилбензола на катализаторах СТК-2М-9 ( 1 и СТК-1-7 ( 2 от температуры. [21] |
Рассчитанные по уравнению (1.2) значения констант скоростей реак-цли показали, что для всех изученных оксидных катализаторов зависимость константы скорости реакции окисления паров изопропилбензола от температуры подчиняется уравнению Аррениуса аналогично процессу окисления на платиносодержащих катализаторах. В качестве примера на рис. 1.3 представлена зависимость константы скорости реакции окисления паров изопропилбензола от температуры в координатах линейной анаморфозы Ink f ( l / T) для двух из исследованных оксидных катализаторов. [22]
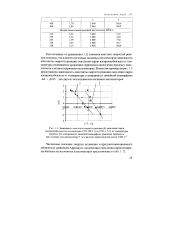 |
Зависимость константы скорости реакции ( k окисления паров изопропилбензола на катализаторах СТК-2М-9 ( 1 и СТК-1-7 ( 2 от температуры. [23] |
Рассчитанные по уравнению (1.2) значения констант скоростей реакции показали, что для всех изученных оксидных катализаторов зависимость константы скорости реакции окисления паров изопропилбензола от температуры подчиняется уравнению Аррениуса аналогично процессу окисления на платиносодержащих катализаторах. В качестве примера на рис. 1.3 представлена зависимость константы скорости реакции окисления паров изопропилбензола от температуры в координатах линейной анаморфозы Ink f ( l / T) для двух из исследованных оксидных катализаторов. [24]
Соли щелочных и щелочноземельных металлов ( 0 1 - 0 2 % в растворе) в 4 - 16 ра з увеличивают константу скорости реакции окисления. Это свойство указанных солей было использовано в технике для получения уксусной кислоты из ацетальдегида: во избежание образования гидроперекиси уксусной кислоты было предложено применять щелочные и щелочноземельные металлы органических кислот. [25]
Метод состоит в том, что реакционная смесь используется в качестве НФ и изменение ее состава контролируется изменением элю-ционных характеристик хроматограф, соединений. Определенная таким методом константа скорости реакции окисления бензаль-дегида в бензойную к-ту равна 4 7 - Ю3 минГ1 в согласии с константой, полученной методом объемного окисления. [26]
Как известно, в горне доменной печи на воздушном и тем более на обогащенном кислородом дутье развиваются очень высокие температуры, порядка 1550 - 1800 С. Это обусловливает высокие значения констант скоростей реакции окисления, порядка k 600 - 1100 см / сек. [27]
Полученные в работе50 значения констант скорости реакции различных стадий показывают, что лимитирующей стадией в синтезе нитрилов является окисление пропилена в альдегиды. Значения кажущейся энергии активации и константы скорости реакции окисления пропилена и суммарного процесса образования нитрилов практически одинаковы. [28]
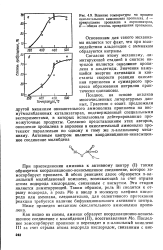 |
Влияние температуры на процесс окислительного аммонолиза пропилена. А - превращение пропилена в акрилонитрил, Б - общая степень превращения пропилена. [29] |
Согласно этому механизму, лимитирующей стадией в синтезе нитрилов является окисление пропилена в альдегиды. Значения кажущейся энергии активации и константы скорости реакции окисления пропилена и суммарного процесса образования нитрилов практически одинаковы. [30]
Страницы: 1 2 3