Экспериментальная константа
Cтраница 2
Здесь k3 - экспериментальная константа скорости, порядок же такой реакции равен четырем. [16]
В газовой фазе экспериментальные константы скорости мало отличаются от расчетных частот соударений радикалов [ 6, с. Снижение скорости рекомбинации радикалов при увеличении их размеров, видимо, связан со стерическими затруднениями, мешающими сближению реагирующих частиц. Частицы с объемистыми заместителями у радикального центра, такие, как ди - и три-трег-бутилметильные или трифенилметильные радикалы, являются вообще долгоживущими. [17]
В результате наблюдаемая экспериментальная константа сверхтонкого взаимодействия уменьшается на множитель cos 28 и становится равной нулю в нулевом поле. [18]
Любые различия в экспериментальных константах должны отражать отличия в конформационной энергии хелатных колец. Рацемический 2 3-диаминобутан способен образовывать хелат с обеими экваториальными метальными группами, но в комплексах других лигандов одна метальная группа должна быть аксиальной. Если термодинамические свойства лигандов в растворе ( например, свободная энергия гидратации) идентичны, то отношение значений / Ci для рацемического лиганда и каждого из двух других лигандов должно быть примерно равно константе равновесия для системы аксиальный метил экваториальный метил, из которой можно рассчитать разность свободных энергий. [19]
Для различных полиэфиров найдены экспериментальные константы и предложены уравнения этого типа, которые приведены ниже. [20]
А и п - экспериментальные константы, G - модуль сдвига, Q - энергия активации ползучести, R - универсальная газовая постоянная, Т - абсолютная температура. Показатель степени п в уравнении ( 1) для интерметаллидов Ni-Al равен трем. [21]
А и В - экспериментальные константы, зависящие от теплофизических свойств полимера. [22]
 |
Изменение эффективной вязкости 10 % - ной суспензии ас-кангсля в процессе нагрева-охлаждения при различных скоростях сдвига. [23] |
А и В - экспериментальные константы, характерные для каждого раствора. [24]
В табл. 16.1 приведены экспериментальные константы скоростей реакций переноса электрона от различных анион-радикалов на пирен в синглетном или триплетом состоянии. В соответствии с термодинамическими характеристиками в случае реакции пирена в сингпетном состоянии константы скоростей увеличиваются при сдвиге окислительно-восстановительных потенциалов анион-радикалов в отрицательную сторону. [26]
На рис. 4.15 приведены экспериментальные константы равновесия легких углеводородных смесей различного состава при температуре 400 К. Из рисунка видно, что константы равновесия для каждой из смесей сходятся к единице при давлении, называемом давлением схождения. [27]
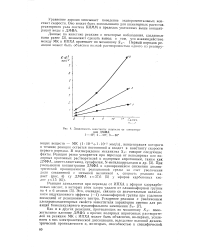 |
Зависимость константы скорости от концентрации ДМФА. 1 - 40. 2 - 50. 3 - 60. [28] |
Уравнение хорошо описывает поведение экспериментальных констант скорости. Оно может быть использовано для инженерных расчетов, реакторного узла синтеза КИММ в пределах указанных выше концентраций воды и ДМФА. [29]
 |
Сравнение / н - Hv молекул с АН. Для радикалов. [30] |
Страницы: 1 2 3 4
