Концентрационная константа - равновесие
Cтраница 1
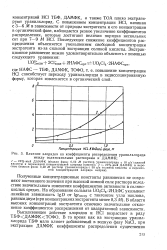 |
Влияние хлоридов на коэффициенты распределения уранилхлорида между солянокислыми растворами и ДАМФК. [1] |
Полученные концентрационные константы равновесия не сохраняют постоянного значения при высокой ионной силе раствора вследствие значительного изменения коэффициентов активности в солянокислых средах. В области высоких концентраций экстрагента отмечено значительное отклонение коэффициентов распределения от квадратичной зависимости. [2]
Концентрационная константа равновесия обменной реакции значительно понижается с уменьшением содержания цезия в твердой фазе при практически равной ионной силе водного раствора. Установлен ряд сродства ионов щелочных металлов к исследованному стеклу ( ряд селективности): Cs K Rb Na, подтверждающий предпочтительность использования солей калия, а не натрия для выщелачивания редких щелочных металлов из вулканических стекол. Кинетика выщелачивания цезия и рубидия из стекол раствором хлористого калия лимитируется внутренней диффузией. [3]
С) - концентрационная константа равновесия, соответствующая реакции (2.3); Кг - константа димеризацни азотной кислоты в органической фазе. [4]
Коэффициенты селективности представляют собой концентрационные константы равновесия, и значения их зависят от ионной силы обеих фаз. Набухание понята затрудняет определение стандартного состояния для ионов, связанных в смоляной фазе. [5]
Эти величины называются концентрационными константами равновесия. [6]
Константа Кс называемая концентрационной константой равновесия, зависит только от температуры. Если какой-либо из реагентов составляет отдельную твердую фазу, его концентрация не фигурирует в выражении константы Кс и условно может быть заменена единицей. Изложенные представления в упрощенной форме могут быть применены полуколичественно к растворам слабых электролитов и для описания состояний равновесия в растворах малорастворимых солей. [7]
В теории равновесий им отвечают концентрационные константы равновесия, которые целесообразней было бы назвать условными, так как они зависят от условий среды. [8]
Фактически коэффициент распределения - это условная концентрационная константа равновесия. [9]
В аналитических расчетах удобнее пользоваться концентрационными константами равновесия в том случае, если они были определены при таких условиях, которые приближаются к условиям действительного применения. [10]
В отдельных случаях индексами служат латинские обозначения соответствующих параметров: например концентрационная константа равновесия обозначается Кс, так как через С обозначаются концентрации, а константа, выраженная через парциальные давления ( р), обозначается К. [11]
Из-за слабого катион-анионного взаимодействия модель комплекса остается под вопросом, а концентрационные константы равновесия имеют, вероятно, малый физический смысл для таких концентрированных растворов электролитов. Тем не менее в некоторых случаях было установлено существование в растворах нитратокомплексов. [12]
Иногда вместо термодинамической константы равновесия (3.9) определенный интерес представляет так называемая концентрационная константа равновесия ОВ реакции Кг - постоянная величина при большом избытке фонового электролита, поскольку в этих условиях коэффициенты активности всех веществ остаются практически постоянными. [13]
В случае приближенных расчетов этими поправками можно пренебречь и принять, что концентрационная константа равновесия не зависит от ионной силы раствора. Для более точных расчетов, однако, желательно вводить поправки везде, где это возможно. [14]
Если побочные реакции отсутствуют, то а 1 и условная константа равновесия совпадает с концентрационной константой равновесия. [15]
Страницы: 1 2 3