Истинная константа - диссоциация
Cтраница 2
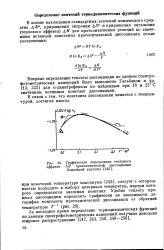 |
Графическое определение теплового. [16] |
Впервые определение теплоты диссоциации по данным спектрофотометрических измерений было выполнено Гальбаном и др. 113, 223 ] для а-динитрофенола по найденным при 18 и 25 С значениям истинных констант диссоциации. [17]
Очевидно, что, исходя из ионной теории индикаторов, можно получить то же уравнение с той лишь разницей, что величина К означала бы не кажущуюся, а истинную константу диссоциации индикатора. [18]
Погрешность в определении истинной константы диссоциации слагается в основном из трех величин: погрешности, вносимой спектрофотометрическими измерениями, погрешности потенциоме-трических измерений ( если они производились) и ошибки, которая вносится принятой методикой нахождения истинной константы диссоциации по найденному значению кажущейся или концентрационной константы диссоциации. [19]
Если ионная сила р, в водном растворе электролита больше нуля, а коэффициент активности не равен единице, то упрощенное вычисление рН приводит к заметным отклонениям от действительных величин, так как в присутствии посторонних ионов истинная константа диссоциации чистой воды Ка не равна Кс. Вследствие того, что ан / н 1Н ], истинное значение водородного показателя равно раНрН - Hg / н Зная состав раствора, можно рассчитать его ионную силу и найти соответствующий коэффициент активности. Поскольку в качественном анализе не применяют точно отмеренных объемов реагентов и концентрации исследуемых растворов не превышают 0 01 - 0 05 М, можно производить расчеты без учета ионной силы раствора. [20]
Уравнение ( VI 1 22) называется законом разбавления Оствальда. Истинная константа диссоциации не зависит от кбнцентрации электролита в растворе ( или от разбавления), а зависит лишь от температуры и природы растворителя. [21]
 |
Кривая потенциометрического титрования слабокислотного катионита щелочью.| Изменение обменной емкости катионитов с изменениием рН раствора. [22] |
Для определения истинной константы диссоциации ионитов предложены более сложные методы расчета. [23]
ТА Hf4ACOOTBeTCTB HHO обозначают коэфициенты активности ионов водорода, анионов и недиссоциированной кислоты. ДА называется термодинамической или истинной константой диссоциации кислоты, а Кс стехиометрической константой. Очевидно, что / Сл является гораздо более полезной и важной константой. Часто возникает недоразумение, какая константа подразумевается, а в таблицах констант они не всегда различаются друг от друга. [24]
Отклонение наблюдается и для угольной кислоты, но причина его иная. Если ввести соответствующую поправку, то истинная константа диссоциации будет Ю-3-6, что близко к ожидаемому интервалу значений. [25]
 |
Диаграмма состояния диоксида углерода. [26] |
Это кажущиеся константы диссоциации, они отнесены к общему количеству растворенного СО2, а не к истинной концентрации НаСОз, которая точно не известна. Но так как молекул Н2СО3 в растворе мало, то истинные константы диссоциации гораздо больше указанных. Равновесие между СО2 и Н2СО3 устанавливается не мгновенно. Молекулы Н2СОз существуют только в растворе. [27]
 |
Диаграмма состояния диоксида углерода. [28] |
Это кажущиеся константы диссоциации, ени отнесены к общему количеству растворенного СО2, а не к истинной концентрации Н2СОз, которая точно не известна. Но так как молекул Н2СОз в растворе мало, то истинные константы диссоциации гораздо больше указанных. Равновесие между СО2 и Н2СО3 устанавливается не мгновенно. Молекулы Н2СОз существуют только в растворе. [29]
В водных растворах сильных электролитов ( кислот и щелочей) ионная сила больше нуля, а коэффициент активности иона водорода не равен единице. В этих случаях упрощенное определение рН приводит к отклонениям от действительных величин, так как в присутствии посторонних ионов истинная константа диссоциации воды не равна константе диссоциации, вычисленной по молярным концентрациям. [30]
Страницы: 1 2 3