Истинная константа - равновесие
Cтраница 1
Истинная константа равновесия зависит только от температуры. Модифицированные константы равновесия, которыми часто пользуются в расчетах, могут зависеть также от давления и состава реакционной смеси. Поэтому при использовании таких констант нужно проявлять осторожность. [1]
Для нахождения истинных констант равновесия р / из мнимых Р / [ уравнение ( 240) ] необходимо знать концентрацию [ В ], которая зависит от СА. [2]
Для определения истинных констант равновесия необходима экстраполяция к бесконечному разбавлению. Несколько более подробно эта проблема рассматривается на стр. [3]
Он отличается от истинной константы равновесия / С. [4]
Если кажущаяся константа равновесия меньше истинной константы равновесия, реакция протекает самопроизвольно в сторону образования продуктов. Когда кажущаяся константа равновесия совпадает с Кр вн) прямая и обратная реакции протекают с одинаковой скоростью и химическая система находится в положении равновесия. [5]
Поскольку кажущаяся константа равновесия Q меньше истинной константы равновесия Кс, система должна самопроизвольно смещаться к равновесию путем образования дополнительного количества NH3 ( см. разд. Обратный процесс, превращение NH3 в N2 и Н2, не является самопроизвольным для указанной смеси реагирующих веществ при 472 К. [6]
Однако эта константа не является истинной константой равновесия, так как она рассчитана через отношение статистических сумм, в которых учтено разное число степеней свободы. [7]
Кр и Кс не являются истинными константами равновесия, если / г / Рг В этом случае константа Кр не только от температуры, но и от давления и от соотношения между компонентами. Так, для реакции синтеза при температуре 457 С Кр увеличивается примерно на 35 % при возрастании от 1 до 300 атм. [8]
Поскольку применение рассмотренных выражений для определения истинных констант равновесия сопряжено со значительными трудностями, при обработке экспериментальных данных, как правило, используют уравнения для кажущихся констант равновесия. [9]
Заключенная в фигурные скобки часть формулы представляет собой истинную константу равновесия / СИст ( 4), когда реагируют неассоциированные частицы. [10]
При произвольно заданных экспериментальных условиях, в тех случаях когда кажущаяся константа равновесия меньше истинной константы равновесия, реакция протекает самопроизвольно в прямом направлении. Если Q больше, чем Кравн, самопроизвольно протекает обратная реакция. [11]
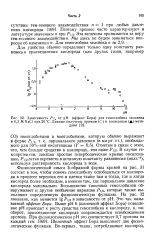 |
Зависимость Р /, от рН ( эффект Бора для гемоглобина человека в 0 3 М NaCl при 20 СС. Данные получены прямым ( С и косвенным ( методами. [12] |
В случае ге-мопротеиков, дающих простые гиперболические кривые оксигенации, Pi / 2 легко перевести в истинную константу равновесия ( моль 1), используя растворимость кислорода в воде. [13]
Для качественной оценки относительной устойчивости комплексов как в основном, так и в возбужденном состоянии используются рассматриваемые значения Лмакс вместо истинных констант равновесия, которые для аддуктов парациклофанов определить не удалось из-за ограниченных количеств доноров. [14]
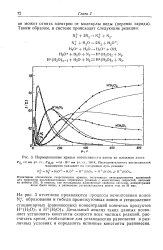 |
Нормированные кривые интенсивности ионов во влажном азоте. [15] |
Страницы: 1 2 3