Истинная константа - равновесие
Cтраница 2
Детальный анализ таких данных позволяет установить константы скорости всех частных реакций, рассчитать время, необходимое для установления равновесия в различных условиях и определить истинные константы равновесия. [16]
Например, в случае трансаминазного механизма, когда первый продукт реакции является конкурентным ингибитором по отношению к второму субстрату, константа конкурентного ингибирования оказывается истинной константой равновесия. [17]
Когда система находится в равновесии, AG должно быть равно нулю, а кажущаяся константа равновесия Q должна, по определению, совпадать с истинной константой равновесия К ( см. разд. [18]
Сравнение констант равновесия, рассчитанных в трех приближениях, показывает, что результат, полученный с помощью первого приближения Улиха, в - 20 раз преувеличивает истинную константу равновесия. В то же время результаты вычислений по второму и третьему приближению мало отличаются друг от друга. Таким образом, применение второго приближения Улиха вполне оправдано при расчетах большинства химических реакций можно не принимать во внимание зависимость молярной теплоемкости от температуры), Расчет по первому приближению дает лишь грубую оценку равновесия. [19]
Поэтому полученная К - это несколько особая константа равновесия, хотя, если определить 8 в соответствии с уравнением ( 58), обе функции совпадают, и К будет представлять собой истинную константу равновесия между реагентами и активированными комплексами. [20]
Подставляя произвольные концентрации реагентов и продуктов в выражение для константы равновесия, как было сделано выше, мы получим кажущуюся константу равновесия, которую обозначают буквой Q. Кажущаяся константа равновесия становится равной истинной константе равновесия К только тогда, когда концентрации всех компонентов реакционной системы достигнут своих равновесных значений, короче говоря, Q К только при равновесии. Мы убедились, что если кажущаяся константа равновесия больше К, то вещества, указанные в правой части химического уравнения реакции, должны реагировать с образованием веществ, указанных в его левой части, другими словами, реакция приближается к равновесному состоянию, смещаясь справа налево. Короче, если Q К, реакция сдвигается справа налево. [21]
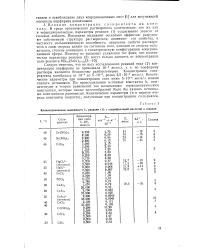
Приведенные расчеты и примеры показывают, что можно установить достаточно надежно уравнение реакции между ионом металла и реактивом. Это является главным в понимании химизма их взаимодействия и основой для вычисления истинных констант равновесия. Что же касается реакций ионов металлов с гидроксил-содержащими реактивами, то описанным не исчерпывается все их многообразие. В частности, материал о взаимодействии ионов металлов с ди - и полифенолами, не способными к таутомерным превращениям, еще недостаточен для обобщений. [22]
Несмотря на то что величины Кз были определены только для двух различных значений 6, данные табл. 1 в этом отношении весьма поучительны. Это указывает на то, что при данных условиях опыта Кз является истинной константой равновесия и что хемосорбция кислорода на палладии локализована на энергетически однородной поверхности и взаимодействие между атомами кислорода не происходит. Тем не менее палладий, по-видимому, занимает в этом отношении промежуточное положение между платиной и никелем. Эти три металла находятся в одной и той же подгруппе периодической системы, однако сродство поверхности никеля к кислороду значительно отличается от соответствующего сродства платины. [23]
Уравнения, определяющие величины Кр и Кс, абсолютно точны при Р - 0, так как только при Р - 0 закон Дальтона, положенный в основу этих уравнений, справедлив для любых газов. В общем же случае КР и Кс, разумеется, не являются истинными константами равновесия: если fiiPi, то КР ( КС) в отличие от Kf будет зависеть не только от температуры, но и от давления, а также и от соотношения между реагентами. [24]
 |
Концентрационная зависимость kv реакции ( 1 с хлорофилловой кислотой в этаноле. [25] |
По происхождению истинные константы kb соответствуют в теории равновесий так называемым термодинамическим константам, которые также целесообразней было бы назвать истинными константами равновесия. [26]
Лишь для вывода К КМ необходимо считать эту комбинацию постоянной, а для расчета термодинамических функций такое предположение необязательно. В соответствии с тем, что kTlnfi представляет собой работу переноса молекулы или иона из чистого растворителя в данный раствор, использование величины К вместо истинной константы равновесия Ка меняет физический смысл рассчитываемой работы мицеллообразования. Здесь нет нестрогости, а есть неточность ( к тому же сравнительно небольшая, см. § 15) в трактовке этой работы как стандартной величины. [27]
Константы скорости реакции в присутствии катализаторов, конечно, могут сильно отличаться от своих значений, характерных для некатализируемой реакции, однако, несмотря на это, отношения констант скорости прямых и обратных реакций должны равняться истинной константе равновесия. Это иногда выражают с помощью известного правила, согласно которому катализатор увеличивает скорость приближения к равновесию, но не может сдвинуть само равновесие. [28]
В литературе описано несколько более или менее специальных методов вычисления констант диссоциации многоосновных кислот ( или многокислотных оснований) по данным титрования. Симе исходит из того факта, что кривая титрования многоосновной кислоты похожа на кривую титрования смеси соответствующего числа одноосновных кислот, и вычисляет ряд констант равновесия реакций титрования особым методом приближения, предположив, что титруемый раствор является смесью одноосновных кислот. Истинные константы равновесия вычисляют из найденных констант равновесия реакций титрования, используя специально выведенные формулы. Метод Симса в общем более сложен и менее удобен, чем описываемый ниже метод, в котором ступенчатые константы определяют непосредственным приближением ряда промежуточных констант. [29]
В литературе описано несколько более или менее специальных методов вычисления констант диссоциации многоосновных кислот ( или много кислотных оснований) по данным титрования. Симе исходит из того факта, что кривая титрования многоосновной кислоты похожа на кривую титрования смеси соответствующего числа одноосновных кислот, и вычисляет ряд констант равновесия реакций титрования особым методом приближения, предположив, что титруемый раствор является смесью одноосновных кислот. Истинные константы равновесия вычисляют из найденных констант равновесия реакций титрования, используя специально выведенные формулы. Метод Симса в общем более сложен и менее удобен, чем описываемый ниже метод, в котором ступенчатые константы определяют непосредственным приближением ряда промежуточных констант. [30]
Страницы: 1 2 3