Электронная конфигурация
Cтраница 1
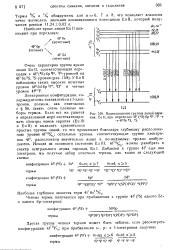 |
Возникновение группы линий европия, Ей 11, при переходах 4f7 ( BS 6р 9Р, Ф - - 4f76s 9S, 7S. [1] |
Электронные конфигурации, содержащие семь эквивалентных f - элек-тронов, должны, как отмечалось в § 56, давать очень сложные наборы термов. [2]
Электронная конфигурация ( 1) возможна, если атом кислорода отдает электрон углероду и образует с ним третью электронную пару. [3]
Электронная конфигурация этого уровня соответствует валентности, равной двум. В этом состоянии молекула должна быть реакциеспособной, а в нормальном состоянии химически инертной. Это очень хорошо соответствует тому, что нам известно о молекулярном азоте, а именно его малой химической активности и трудности его активирования. [4]
Электронные конфигурации и основные состояния некоторых dn конфигураций в октаэдрических и тетраэдрических координационных системах, приведены в табл. V. [5]
Электронные конфигурации и основные состояния некоторых dn конфигураций в октаэдрических и тетраэдрических координационных системах, вполне приемлемые и в аспекте теории кристаллического поля, приведены в табл. III. [6]
Электронная конфигурация, соответствующая наинизшей энергии, должна поэтому быть такой, при которой связывающая орбита ( или орбиты) окажется дважды занятой, а оставшиеся два электрона займут две вырожденные несвязывающие орбиты. Такая конфигурация приводит к трем синглетным и одному триплетному состояниям, из которых последнее, согласно правилу Хунда, должно быть наиболее стабильным. Таким образом, ни одна из этих молекул при правильной плоской форме не будет обладать в основном состоянии замкнутой оболочкой; это обстоятельство, несомненно, связано с неустойчивостью обеих молекул. Позднее мы вернемся к этому вопросу. [7]
 |
Форма связывающих ( слева и разрыхляющих ( справа орбиталей молекулы формальдегида. [8] |
Электронная конфигурация строится путем распределения электронов по орбиталям, имеющимся у системы. В основном, или самом нижнем, энергетическом состоянии электроны должны занять орби-тали, самые низкие по энергии. [9]
Электронная конфигурация представлена совокупностью всех электронов, введенных в диаграмму до символа данного элемента. [10]
Электронная конфигурация представлена как совокупность всех предшествующих электронов, показанных на схеме ниже символа данного элемента. [11]
Электронная конфигурация ns 2np4 дает возможность элементам этой группы проявлять степени окисления - II, 11, IV и VI. Так как до образования конфигурации инертного газа не достает всего двух электронов, то степень окисления - II возникает очень легко. Это особенно характерно для легких элементов группы. Действительно, кислород отличается от всех элементов группы легкостью, с которой его атом приобретает два электрона, образуя двухзарядный отрицательный ион. Для остальных элементов группы отрицательная степень окисления становится постепенно менее устойчивой, а положительные - - более устойчивыми. У тяжелых элементов преобладают низшие положительные степени окисления. [12]
Электронная конфигурация ns2np дает возможность элементам этой группы проявлять степени окисления - II, 11, IV и VI. Так как до образования конфигурации инертного газа недостает всего двух электронов, то степень окисления - II возникает очень легко. Это особенно характерно для легких элементов группы. Действительно, кислород отличается от всех элементов группы легкостью, с которой его атом приобретает два электрона, образуя двухзарядный отрицательный ион. [13]
Электронная конфигурация ns np дает возможность элементам этой группы проявлять степени окисления - II, 11, IV и VI. Так как до образования конфигурации инертного газа не достает всего двух электронов, то степень окисления - II возникает очень легко. Это особенно характерно для легких элементов группы. Действительно, кислород отличается от всех элементов группы легкостью, с которой его атом приобретает два электрона, образуя двухзарлдный отрицательный ион. За исключением необычных отрицательных степеней окисления кислорода в перекисях ( - I), надперекисях ( - У2) и озонидах ( Уз), соединениях, в которых есть связи кислород - кислород, а также состояний 1 и 11 в соединениях O2F2 и OF2 кислород во всех соединениях имеет степень окисления - II. Для остальных элементов группы отрицательная степень окисления становится постепенно менее устойчивой, а положительные - более устойчивыми. У тяжелых элементов преобладают низшие - положительные степени окисления. [14]
Электронная конфигурация - распределение электронов по атомным или молекулярным орбиталям; определяется указанием занятых орбиталей и соответствующих им чисел заполнения. [15]
Страницы: 1 2 3 4 5