Электронная конфигурация
Cтраница 2
Электронная конфигурация охватывает в общем случае несколько состояний атома, отличающихся взаимной ориентацией орбитальных и спиновых моментов электронов. В центральном поле энергия электронов не зависит от ориентации их моментов. [16]
Электронная конфигурация определяет основные химические свойства этих элементов. [17]
Электронные конфигурации 5 / 7 или 4 / 7, представляющие собой наполовину заполненные / - оболочки кюрия и гадолиния, обладают особой устойчивостью. Вот почему трехвалентный кюрий и гадолиний очень устойчивы. В итоге тербий и особенно берклий могут легко окисляться от трехвалентного до четырехвалентного состояния. По-иному этот факт проявляется в случае европия ( и в меньшей степени самария), расположенного непосредственно перед гадолинием. Оба они предпочитают иметь структуру 4 / 7 с более устойчивым, чем обычно, двухвалентным состоянием. Этот факт позволяет предсказать наличие двухвалентного состояния у элемента 102 - предпоследнего элемента из ряда актинидов. [18]
Электронная конфигурация может изменяться при переходе от одного соединения к другому или даже при изменении физического состояния данного соединения. [19]
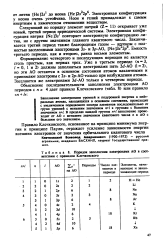 |
Порядок заполнения электронами АО в соответствии с правилом Клечковского. [20] |
Электронная конфигурация у неона очень устойчива. [21]
Электронная конфигурация ns np4 дает возможность элементам этой группы проявлять степени окисления - II, П, IV и VI. Так как до образования конфигурации инертного газа не достает всего двух электронов, то степень окисления - II возникает очень легко. Это особенно характерно для легких элементов группы. Действительно, кислород отличается от всех элементов группы легкостью, с которой его атом приобретает два электрона, образуя двухзарлдный отрицательный ион. За исключением необычных отрицательных степеней окисления кислорода в перекисях ( - 1), надперекисях ( - 1 / 2) и озонидах ( 1 / 3), соединениях, в которых есть связи кислород - кислород, а также состояний 1 и П в соединениях O2F2 и OF2 кислород во всех соединениях имеет степень окисления - II. Для остальных элементов группы отрицательная степень окисления становится постепенно менее устойчивой, а положительные - более устойчивыми. У тяжелых элементов преобладают низшие положительные степени окисления. [22]
Электронная конфигурация 3d9 вызывает сильные искажения обычной для переходных металлов октаэдрической структуры координационных сфер. Геометрически он представляет собой искаженный октаэдр ( см. рис. 23.2, в), в котором две молекулы воды, находящиеся одна напротив другой на одной из осей октаэдра, больше удалены от катиона Си2, чем остальные четыре, а их связи с катионом слабее. [23]
Электронная конфигурация sl определяет положение элемента в первой группе, но высокий ПИ и возможность образования иона Н - сближает его с галогенами. Гелием заканчивается первый период. Полностью застроенный электронный jfiC - слой высокий: потенциал ионизации, суммарный спин, равный нулю, - все это обусловливает особую устойчивость электронной оболочки гелия, его химическую инертность и диамагнетизм его атомов. [24]
 |
Схемы заполнения МО мо лекул, образованных атомами 1-го периода. [25] |
Электронная конфигурация в основном состоянии Hatfe I) 2 ] - В основном состоянии молекулы два ее электрона согласно принципу наименьшей энергии: занимают наиболее низкую орбиталь al s и согласно запрету Паули имеют противоположные спины. Суммарный спин равен нулю, молекула должна быть диамагнитна - что и наблюдается. [26]
Электронная конфигурация каждого из четырех галогенов - фтора, хлора, брома и иода - стабилизируется за счет того, что либо атом галогена приобретает электрон ( тем самым полностью заполняется высший р-под-уровень) и превращается в анион Х -, либо атом галогена образует одинарную связь. [27]
Электронная конфигурация каждого из четырех галогенов - фтора, хлора, брома и иода - стабилизируется за счет того, что либо атом галогена приобретает электрон ( тем самым полностью заполняется высший р-под-уровень) и превращается в анион X, либо атом галогена образует одинарную связь. [28]
Электронная конфигурация и геометрическая форма переходного комплекса могут ограничиваться запретами по симметрии. При образовании переходного комплекса происходит перекрывание орбиталей. Этот процесс возможен лишь при условии, что ор-битали имеют одинаковую симметрию. В противном случае процесс тормозится из-за очень большой энергии активации. Энергия колебаний атомов в молекуле может принимать различные значения, однако она не может быть меньше нулевой энергии. Если бы энергия равнялась нулю, то скорость движения атомов тоже обратилась бы в нуль и мы могли бы точно определить координату атома, а это в силу принципа неопределенности невозможно. [29]
 |
К Вопросу - 55. [30] |
Страницы: 1 2 3 4 5