Диаграмма - растворимость - система
Cтраница 2
На рис. 68 показана диаграмма растворимости системы, обладающей нижней КТР. Следует иметь в виду, что в некоторых случаях достижению нижней КТР мешает замерзание одной из жидкостей, а достижению верхней КТР препятствует переход в критическое состояние одного из компонентов. [16]
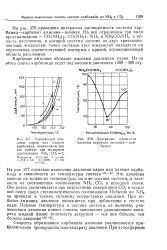 |
Диаграмма плавкости.| Равновесное давление паров над плавом карбамида, получаемым при его синтезе при молярном соотношении NH3. СО2 2. [17] |
На рис. 376 приведена диаграмма растворимости системы карбамид-карбамат аммония-аммиак. На ней ограничены три поля кристаллизации - СО ( NH2) 2, CO ( NH2) - NH3 и NH2CO2NH4, и область расслоения, в которой система состоит из двух трехкомпо-нентных жидкостей; точки составов этих жидкостей находятся на пересечении соответствующей изотермы с кривой, ограничивающей область расслоения. [18]
На рис. 57 приведена диаграмма растворимости системы карбамат аммония - вода. [19]
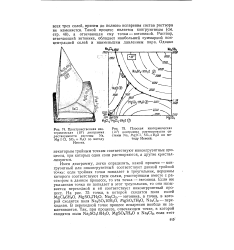 |
Пространственная изотермическая ( 10 диаграмма. растворимости системы Na, Mg 11 Cl, SO4 H20 по методу Иенеке. [20] |
Плоская изотермическая ( 10) диаграмма растворимости системы Na, MgilCI, S04 H2O по методу Иенеке. [21]
На рис. 62 показан вид диаграммы растворимости системы, обладающей нижней КТР. [22]
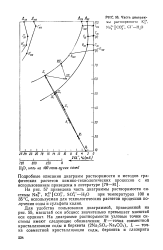 |
Часть диаграммы растворимости К. [23] |
На рис. 57 приведена часть диаграммы растворимости системы Nal, кПСОз, SOV - Н2О при температурах 100 и 35 С, используемая для технологических расчетов процессов получения соды и сульфата калия. [24]
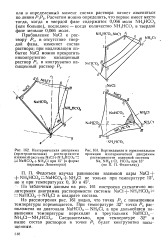 |
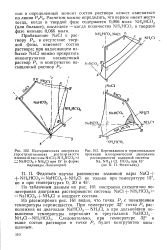
Изотермическая диаграмма ( пространственная растворам ости взаимной системы NaCl NH4HCO3 - J2NaHCO3 - - NH4Cl при 15 ( в форме пирамиды Левенгерца. [25] |
По табличным данным на рис. 161 построена схематично по-литермная диаграмма растворимости системы NaCl 4 - NH4HCO3 NaHCOg - f - NH4C1 в квадрате состава. [26]
 |
Изотермическая диаграмма ( прэстранственная растворимости взаимной системы NaCl NH4HCO3 - NaHCO3 - - NH4Cl при 15 ( в форме пирамиды Левенгерца. [27] |
По табличным данным на рис. 161 построена схематично по-литермная диаграмма растворимости системы NaCl - j - Nh HCOg - - NaHCO3 - f - NH4C1 в квадрате состава. [28]
Опытные данные изопиестических измерений можно изобразить на диаграмме растворимости системы из воды и двух солей с общим ионом в виде совокупности фигуративных точек, каждой из которых соответствует определенное значение активности воды в растворе. Необходимо, чтобы таких точек было достаточно много и. [29]
Рассмотрим процесс упаривания раствора VII, пользуясь диаграммой растворимости системы Na K l CO - Cl - - Н2О ( см. ркс. Упаривание раствора пр-и 100 С влечет за собой перемещение фигуративной его точки на диаграмме растворимости этой системы по лучу кристаллизации соды до точки VIII, расположенной на границе полей кристаллизации соды и хлорида калия. [30]
Страницы: 1 2 3 4