Концентрация - анион - кислота
Cтраница 1
Концентрация анионов кислоты Ап - постоянна, а концентрация катионов основания Kt в продолжение титрования увеличивается. Кривая титрования имеет V-образную форму, характерную для процесса нейтрализации сильных кислот сильными основаниями. При этом первоначальная ветвь кривой, соответствующая уменьшению концентрации ионов водорода до точки эквивалентности, имеет более острый угол наклона, чем ветвь кривой, характеризующая повышение концентрации гидроксильных ионов после окончания процесса нейтрализации. [1]
Здесь концентрация анионов кислоты принимается равной концентрации добавленной щелочи, а концентрация молекул кислоты равна разности между общей концентрацией и концентрацией анионов. [2]
Высота второй волны определяется концентрацией анионов кислоты вблизи электрода. Изучение зависимости высот волн от рН раствора и сопоставление этих величин с величинами предельных диффузионных токов дает данные, достаточные для вычисления констант скоростей химических реакций, предшествующих разряду. [3]
Высота второй волны определяется концентрацией анионов кислоты вблизи электрода. Изучение зависимости высот волн от рН раствора и сопоставление этих величин с величинами предельных диффузионных токов позволяет получить исходные данные, необходимые для вычисления констант скоростей химических реакций, предшествующих разряду. [4]
Высота второй волны определяется концентрацией анионов кислоты - вблизи электрода. Изучение зависимости высот волн от рН раствора и сопоставление этих величин с величинами предельных диффузионных токов позволяет получить исходные данные, необходимые для вычисления констант скоростей химических реакций, предшествующих разряду. [5]
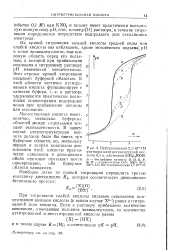 |
Нейтрализация 2 1 - 10 - 3М раствора нитрилтриуксусной кислоты 0 1 н. раствором ( CHS 4NOH. [6] |
При титровании слабой кислоты сильным основанием концентрация анионов кислоты ( в нашем случае Х -) равна оттитрованной доле кислоты. [7]
При титровании слабой кислоты сильным основанием концентрация анионов кислоты равна оттитрованной доле кислоты. [8]
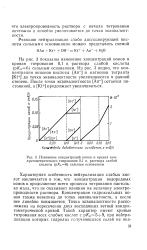 |
Изменение концентраций ионов и кривая кон. [9] |
Из рис. 3 видно, что концентрации анионов кислоты [ An - ] и катионов титранта [ Kt ] до точки эквивалентности увеличиваются в равной степени. После точки эквивалентности [ Ап - ] остается постоянной, a [ Kt ] продолжает увеличиваться. [10]
При титровании слабой кислоты сильным основанием концентрация анионов кислоты равна оттитрованной доле кислоты. [11]
Концентрация анионов [ A-J слагается из концентраций анионов кислоты и анионов соли. [12]
Концентрация анионов [ А ] слагается из концентраций анионов кислоты и анионов соли. [13]
Концентрация анионов СН3СОО - в растворе слагается из концентрации анионов кислоты и соли. Но степень диссоциации уксусной кислоты весьма мала, а в присутствии соли, дающей одноименный анион, она еще более снижается и практически становится весьма незначительной величиной. [14]
Концентрация анионов [ An - ] слагается из концентраций анионов кислоты и анионов соли. [15]
Страницы: 1 2 3