Концентрация - анион - кислота
Cтраница 2
Концентрация анионов [ А - ] слагается из концентраций анионов кислоты и анионов соли. [16]
Концентрация анионов [ Ап - ] слагается из концентраций анионов кислоты и анионов соли. [17]
Концентрация анионов [ А - ] слагается из концентраций анионов кислоты и анионов соли. [18]
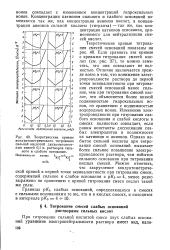 |
Теоретические кривые кондуктометрического титрования сильной кислотой двухкомпонент-ных смесей 0 1 н. растворов сильного и слабого основания. Подвижности ионов. Я.. Я. [19] |
Концентрации катионов сильного и слабого оснований изменяются так же, как концентрации анионов кислот, а концентрация анионов сильной кислоты ( титранта) - так же, как концентрация катионов основания, применяемого для нейтрализации смесей кислот. [20]
Показано, что реакция образования амида является реакцией первого порядка по концентрации аниона карбонрвой кислоты и нейтральной формы амина, причем порядок реакции не зависит от величины рН, поскольку рН определяет состояние ионизации реагентов. Из табл. 1 - 21 видно, что скорость образования амида в заметной степени зависит от структуры амида и карбоновой кислоты. Различие между реакционными способностями уксусной, пропионовой и масляной кислот по сравнению с янтарной кислотой выра жено в меньшей степени. Это указывает на то, что соседний карбокси-лат-анион не участвует в образовании амида. Аналогично скорость реакции с Метиламином значительно выше скорости той же реакции с аммиаком; отношение скоростей реакций при 75 8 равно 11 для пропионовой кислоты и 6 для нзомасляной кислоты. [21]
 |
Полярографические кривые фенилглиоксалевой кислоты в буферах с рН от 2 2 до 9 24. Значения потенциалов полуволн отнесены к н. к. э. [22] |
Ка - отрицательный десятичный логарифм константы диссоциации Ка, [ А - ] - концентрация анионов кислоты и [ НА ] - концентрация недиссоциированных молекул кислоты. [23]
 |
Полярографические кривые фенилглиоксалевой кислоты в буферах с рН от 2 2 до 9 24. Значения потенциалов полуволн отнесены кн. к. э. [24] |
Со - отрицательный десятичный логарифм константы диссоциации Ка, [ А - ] - концентрация анионов кислоты и [ НА ] - концентрация недиссоциированных молекул кислоты. [25]
Таким образом, можно прийти к выводу, что при титровании слабых кислот ( рКа 5) слабым основанием ( р / Сь 5) изменение электропроводности раствора вызывается только повышением концентрации анионов кислоты и катионов основания. Если реакция между слабыми электролитами протекает количественно, концентрации этих ионов при титровании равны между собой, линейно повышаются до точки эквивалентности и остаются постоянными после нее. [26]
При этом следует концентрацию водородных ионов заменять на концентрацию гидроксильных ионов и, наоборот, вместо концентрации анионов титруемой кислоты брать катионы титруемого основания, а вместо концентрации катионов титранта подставлять концентрацию анионов кислоты, используемой при нейтрализации. [27]
Причем все рассуждения в отношении концентрации водородных ионов следует отнести к концентрациям гидроксильных ионов и, наоборот, рассуждения, касающиеся концентрации анионов определяемой кислоты, - к концентрации катионов титруемого основания, а концентрации катионов титранта - к концентрации анионов кислоты, применяемой в процессе нейтрализации основания. Однако кривые титрования оснований и кривые титрования кислот такой же силы несколько отличаются друг от друга. [28]
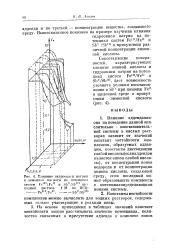 |
Влияние гидроокиси натрия и лимонной кислоты на потенциал систем Fe1II / Fo11 и Sbv / Sbni ( исходный раствор 1 М по НС1. - - - - - - - - - Sbv / Sbm. [29] |
Влияние аддендаани-она на поведение данной окислительно - восстановительной системы в кислых растворах зависит от значений констант нестойкости комплексов, образуемых адден-дом, константы диссоциации слабой кислоты ( если аддендом является анион слабой кислоты), от концентрации ионов водорода и от концентрации аниона кислоты, создающей среду, если последний может образовывать комплексы с потенциалопределяющими ионами системы. [30]
Страницы: 1 2 3