Концентрация - ион - цинк
Cтраница 2
Для того чтобы вычислить концентрацию ионов цинка, оставшихся в растворе после осаждения ZnS, надо знать концентрацию ионов водорода и сульфид-иона. [16]
КЭ), то понижение концентрации ионов цинка в растворе вызовет соответствующее уменьшение силы тока, и весь процесс будет совершенно аналогичен процессу последовательного снятия полярограмм ряда растворов солей цинка различной концентрации. [17]
КЗ), то понижение концентрации ионов цинка в растворе вызовет соответствующее уменьшение силы тока, и весь процесс будет совершенно аналогичен процессу последовательного снятия полярограмм ряда растворов солей цинка различной концентрации. [18]
 |
Устройство водородного электрода. [19] |
Таким образом, с увеличением концентрации ионов цинка потенциал сдвигается в положительную сторону, уменьшаясь по своей абсолютной величине. [20]
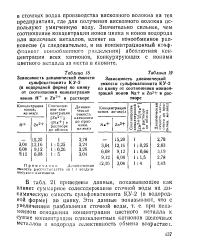 |
Зависимость динамической емкости. [21] |
Значительно сильнее, чем соотношение концентрации ионов цинка и ионов водорода или щелочных металлов, влияет на ионообменное равновесие а следовательно, и на концентрационный коэффициент ионообменного разделения) абсолютная концентрация всех катионов, конкурирующих с ионами цветного металла за места в иноните. [22]
Происходящее в результате растворения повышение концентрации ионов цинка у электрода оказывается, по-видимому, недостаточным для возникновения новых зародышей, поскольку длительность протекания тока в анодном направлении в каждый период не превышает 1 / 100 сек. Вместе с тем, растворение мржет активировать поверхность граней кристаллов, за счет чего в следующий этап отложение металла происходит на гранях того же кристалла. [23]
Линия критических ( пороговых) концентраций ионов цинка лежит значительно выше ( кривая 2), так как коэффициент их диффузии значительно меньше. Коагуляция вискозы происходит через некоторый промежуток времени А / р0 после достижения пороговой концентрации. Этот период времени, обычно называемый периодом индукции, необходим для образования центров структурообразования. Кривая 3, отстоящая на расстоянии ро от граничной линии пороговых концентраций, обозначает линию коагуляции. До точки В коагуляция пропс-ходит в присутствии ионов цинка, и обра-зуется структура волокна типа оболочки. Далее линия коагуляции опережает линию пороговых концентраций Zn-ионов, и осаждение ксантогената идет без их структурообразующего влияния, только за счет нейтрализации и десольватации. Ниже точки В образуется ядро. [24]
Для того что бы вычислить концентрацию ионов цинка, оставшихся в растворе после осаждения ZnS, надо знать концентрацию ионов водорода и сульфид-иона. [25]
Из этих уравнений следует, что повышение концентрации ионов цинка и понижение температуры будут способствовать повышению выхода по току цинка. Повышение катодной плотности тока также должно повышать выход по цинку. Выход по току цинка уменьшается не только из-за катодного выделения водорода, но также из-за наличия в электролите примесей. Такими примесями могут быть соединения кадмия, алюминия, титана, германия, сурьмы, мышьяка, железа, кобальта, никеля и меди. Наиболее вредной примесью является германий. Уже при содержании германия 1 мг / л осаждения цинка не происходит. Поэтому при наличии германия электрод покрывается тонкой пленкой этого металла, которая легко окисляется, превращаясь в почти неэлектропроводную двуокись германия. Последняя блокирует поверхность электрода, благодаря чему электроосаждение цинка почти прекращается. [26]
С при 6000 аЛи2 еще не страшны; изменение концентрации ионов цинка в пределах 30 - 60 г / л практически не влияет на выход по току при 6000 а / м и достаточном перемешивании. Для получения высоких выходов по току электролит должен быть исключительно чистый. [27]
 |
Электродные потенциалы меди и цинка в цианистых электролитах. [28] |
Как видно, совместный разряд с приведенным здесь соотношением концентраций ионов цинка и меди практически немыслим. [29]
 |
Электродные потенциалы меди и цинка в цианистых электролитах. [30] |
Страницы: 1 2 3 4