Концентрация - ион - цинк
Cтраница 3
Как видно, совместный разряд с приведенным здесь соотношением концентраций ионов цинка и меди практически немы - - слим. [31]
Пробу исследуемого раствора увеличивают до 5 капель для того, чтобы повысить концентрацию ионов цинка в колонке, так как раствор после осаждения нерастворимых оснований становится сильно разбавленным, а концентрация ионов цинка ничтожной. [32]
Легко подать, почему щелочные металлы разлагают воду с образованием щелочных ионов и почему концентрация ионов цинка при аналогичных условиях очень мала. Вода же ионизирована весьма слабо; ее ионное произведение, как указано на стр. Окислительный потенциал водорода по отношению к такому очень разбавленному раствору ионрв водорода равен не 0 0, как указано: в табл. 10, но приближается по величине к потенциалу ции-ка; он был бы примерно равен последнему, если бы ионное произведение воды было равно ] - ге. В соответствии с окислительными потенциалами мы должны ожидать, что цинк будет разлагать воду с выделением водорода. Действительно, цинк в соприкосновении с водой несколько окисляется ( причем окисляющим агентом является водород воды), но реакция не достигает каких-либо заметных размеров. Первыми продуктами реакции являются ионы цинка и свободный водород, но за счет удаления ионов водорода в растворе появляется избыток свободных пидроксил-иоиов. Произведение растворимости гидроокиси цинка согласно табл. 8 ( стр. Образующийся на поверхности металлического цинка слой нерастворимой гидроокиси защищает его, предотвращая дальнейшее растворение. Если же водород находится в виде кислоты, с анио. [33]
С повышением концентрации цианида в растворе концентрация ионов меди уменьшается в большей степени, чем концентрация ионов цинка. Если к тому же учесть, что катодная поляризация более резко выражена при осаждении меди, чем при осаждении цинка, то становится очевидным, что имеется полная возможность управлять процессом совместного осаждения на катоде двух таких отличных в электрохимическом отношении металлов, как медь и цинк. [35]
Расхождение для системы цинк - - ион цинка, всего вероятнее, обусловливается ненадежными данными о концентрации ионов цинка вследствие загрязнения индикатора изотопами. Расхождения для системы серебро-ион серебра, вероятнее всего, объясняется необоснованностью предположения о том, что термодинамическая активность для осадка индикатора равна единице, хотя неясно, почему это предположение для серебра оправдывается, если осадок отлагается на платине в щелочном растворе цианида, но не оправдывается, если осаждение происходит в растворах гидроокиси аммония или азотнокислого калия. Необходимо продолжить исследования термодинамической активности индикаторного-осадка. [36]
Для последующего демаскирования ионов обоих металлов необходимо снизить концентрацию цианид-ионов приблизительно до 10 4 М, вследствие чего концентрация ионов цинка возрастает до 10 - 6 М и, как видно из рис. 25, при pZn 6 эриохром черный Т будет присутствовать в виде красного комплекса с цинком. Это понижение концентрации цианид-ионов от 10 - 2 до 10 - 4 часто легко достигается при применении альдегида. [37]
Заметим, что для цинкового электрода o Zn столь значительна, что физически невозможно получить в растворе такую концентрацию ионов цинка, поэтому всегда a Za Zn и потенциал цинкового электрода всегда положителен. [38]
 |
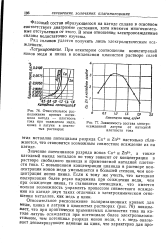
Расход электроэнергии на эле. С троосаждение цинка в зависимости от кислотности раствора и плотности тока. [39] |
Напряжение на ванне уменьшается при сближении электродов, при увеличении концентрации кислоты, с повышением температуры; мало изменяется от концентрации ионов цинка и растет с увеличением плотности тока. [40]
В случае амальгамы цинка количественные опыты велись в присутствии тетрабутиламмония и было показано, что скорость выделения металла iK не зависит от концентрации ионов цинка в растворе. [41]
У обоих типов электродов устойчивое значение потенциала устанавливалось через 10 - 15 мин, в то время как электрод с жидкой мембраной реагировал на изменение концентрации иона цинка в течение 1 мин. [42]
Определив активность ионов гидроксила и имея в виду, что произведение растворимости не зависит от концентрации электролита, можно определить активность, а затем и концентрацию ионов цинка. [43]
Пробу исследуемого раствора увеличивают до 5 капель для того, чтобы повысить концентрацию ионов цинка в колонке, так как раствор после осаждения нерастворимых оснований становится сильно разбавленным, а концентрация ионов цинка ничтожной. [44]
При использовании сульфокатионита КУ-2 в Н - форме динамическая обменная емкость катионита по иону цинка до проскока составляет 2 - 3 мг-экв / г ( воздушно-сухого катионита), причем соотношение концентрации ионов цинка и ионов водорода или щелочных металлов мало влияет на обменную емкость катионита [ 89, с. Увеличение общей минерализации воды резко снижает емкость сульфокатионитов. [45]
Страницы: 1 2 3 4