Концентрация - ион - цинк
Cтраница 4
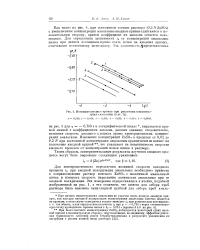 |
Истинные анодик. е кривые при различных концентрациях амальгамы ( ват. %. [46] |
Изменение концентрации ZnSO в пределах от 0 02 до 0 3 N при постоянной концентрации амальгамы практически не влияет на положение анодной кривой, что указывает на независимость скорости анодного процесса от концентрации ионов цинка в растворе. [47]
При равновесии отношение активностей ионов цинка и меди приблизительно равно отношению концентраций при тех же условиях; следовательно, когда система, состоящая из цинка, меди и их двухвалентных ионов, достигает равновесия, то отношение концентраций ионов цинка и меди крайне велико. [48]
Если, например, в каломельной цепи хлористую закись ртутл, рассматриваем, ю в данном случае как вещество нерастворимое, заменить относительно легко растворимой хлористой закисью таллия, то следует п; инять во внимание, что концентрации ионов цинка и хлора не находятся более в одном и том же отношении в обоих растворах. Ибо к ионам хлора, из хлористого цинка, прибавляются еще хлор-ионы, из хлористой закиси таллия, причем, согласно закону действия масс, по которому произведение концентрации ионов таллия и хлора в насыщенном растворе хлористой закиси таллия должно быть постоянным, этот прирост ионов хлора в разбавленном растворе хлористого цинка ольше, 1 ем в концентрированном. Если через р и рг обозначить осмотические давления или концентрации ионов цинка, а через р и р те же величины для ионов хлора, то, приним. [49]
Так как электролит ZnS является менее растворимым, в колонке будет выпадать только белый осадок сульфида цинка; он выпадает до тех пор, пока в растворе над осадком концентрация ионов железа станет в 4 8 - 105 раз больше концентрации ионов цинка. [50]
В соответствии с (9.6) SH, в ходе реакции будет уменьшаться, так как в постоянном объеме будет накапливаться все большее количество водорода и тем самым объем, приходящийся на 1 моль, будет уменьшаться; 5Z ( 12 будет уменьшаться в соответствии с (9.9), поскольку концентрация ионов цинка растет, а SH будет расти в соответствии с той же формулой в силу уменьшения концентрации ионов Н; SZn изменяться не будет, так как цинк - компонент, образующий фазу постоянного состава, и его молярные характеристики не изменяются. В итоге можно прийти к выводу, что AS по мере превращения убывает. [51]
Образовавшиеся при этом ионы цинка ничем не отличаются от ионов цинка, поступивших в раствор с электрода. Повышение концентрации ионов цинка в электролите облегчает переход этих ионов в металл из раствора и затрудняет переход из металла в раствор. Поэтому в растворе цинкового купороса погруженный цинковый электрод хотя и заряжается отрицательно, но слабее, чем в чистой воде. [52]
С; II концентрация ионов цинка 35 г / л, плотн. С; III концентрация ионов цинка 35 г / л кислоты 150 г / л, плотн. IV концентрация кислоты 160 г / л, плотн. [53]
 |
Стандартные электрохимические потенциалы некоторых элементов при 25 С по отношению к стандартному водородному электроду. [54] |
Напряжение гальванического элемента может изменяться в зависимости от концентрации находящегося в нем электролита. Например, изменяя концентрацию ионов цинка в цинковом полуэлементе, мы сместим, согласно принципу Ле Ша-телье, равновесие между цинком и ионами цинка, и вследствие этого изменится электродный потенциал цинка. При [ Zn2 ] 1 моль / л стандартный потенциал этого электрода равен 0 76 В, но при уменьшении [ Zn2 ] равновесие Zn Zn2 2e - смещается в правую сторону, а поскольку электродный потенциал является мерой способности реакции к самопроизвольному протеканию, ясно, что в данной ситуации он должен возрасти. [55]
После прохождения точки эквивалентности концентрация ионов цинка в присутствии A1Y - изменяется менее быстро, потому что А13 частично вытесняется из его комплекса ионами цинка. [56]
Прямую, подобную приведенной на рис. 1 6, можно получить экспериментально: совершенно очевидно, что если к раствору, содержащему, например, 3 2 мг цинка ( случай, изображенный на рис. а, кривая 1), будем добавлять какой-либо осадитель и тем самым постепенно понижать концентрацию цинка в растворе, предва1рительно установив потенциал электрода так, чтобы он находился в пределах площадки предельного тока, например - 1 65 В ( Нас. КЭ), то понижение концентрации ионов цинка в растворе вызовет соответствующее уменьшение силы тока, и весь процесс будет совершенно аналогичен процессу последовательного снятия подпрограмм ряда растворов солей цинка различной концентрации. [57]
Характерным примером этого служит осаждение цинка из цинк-сульфатной ванны. При содержании 300 г / л сульфата цинка концентрация ионов цинка теоретически соответствует приблизительно одномолярному раствору. [58]
 |
Влияние температуры. [59] |
Поэтому покрытия, полученные в цианистых электролитах, более мелкокристалличны. С повышением в электролите концентрации цианида и щелочи концентрация ионов цинка понижается, возрастает катодная поляризация. Изменение относительной концентрации в электролите цианида и щелочи влияет на качество цинковых покрытий. [60]
Страницы: 1 2 3 4