Концентрация - кетон
Cтраница 3
 |
Зависимость экстракции селена от кислотности среды. [31] |
Исследовано взаимодействие селена ( 1У) с ацетоном, метилэтилкетоном, диэтилкетоном, метилпропилкетоном, метилизопронилкетоном, метилизо-бутилкетоном и ацетофеноном в зависимости от концентрации кетона и от времени. В сернокислой среде реакция не идет. [32]
 |
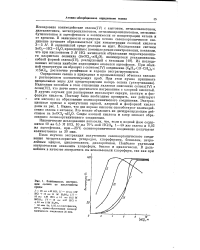
Влияние условий депарафинизации и промывки на результаты процесса. [33] |
Применение растворителя переменного состава не влечет технологических трудностей, так как при регенерации кетон-аромати-ческого растворителя в парах, уходящих из первой ступени регенерации, концентрация кетона повышается, в то время как пары следующих ступеней регенерации растворителя содержат больше ароматического компонента. Ниже приведены данные о содержании кетона при регенерации растворителя из раствора фильтрата на одной из установок обезмасливания Грозненского НПЗ им. [34]
Параллельно происходит конденсация двух молекул кетона, поэтому для повышения выхода целевого продукта лучше проводить процесс в растворе и под давлением ацетилена, чтобы концентрация кетона была сравнительно низкой, а концентрация ацетилена высокой. [35]
Эта реакция, как и галоформная реакция ( см. 10.6), катализируется и основаниями и кислотами; в каждом случае скорость реакции зависит от концентрации кетона и кислоты или основания, но не зависит от концентрации галоида. [36]
Бензол и толуол хорошо растворяют парафины и церезины при низких температурах; поэтому их присутствие в растворителе увеличивает температурный градиент депарафинизации и тем больше, чем меньше концентрация кетона в растворителе. [37]
При применении некоторых полярных растворителей ( ацетон, дихлорэтан и др.) введение модификаторов кристаллической структуры не требуется, так как в присутствии этих растворителей образуются сложные формы кристаллов парафина. Так, лкшмше-ние концентрации кетона в смеси с толуолом способствует проте-дсалию. [38]
Оксигидроперекись распадается на радикалы быстрее, чем перекись водорода. С ростом концентрации кетона увеличивается доля перекиси, которая находится в форме оксигидро-перекиси, соответственно растет скорость образования радикалов. [39]
Полосы поглощения карбоновых кислот и кетонов не разрешаются спектрометром. Определив в отдельном опыте концентрацию кислот титрованием, вычисляют концентрацию кетонов. [40]
Существует ряд реакций превращения органических соединений, по скорости которых можно определять концентрации кетонов, сложных эфиров и других соединений. [41]
Как видно из рисунка, расчетная кривая идет несколько выше кинетической кривой накопления Н202, что объясняется неточностью допущения о равенстве концентраций кетона и перекиси водорода. Проведенный расчет еще раз подтверждает правильность представлений о механизме окисления циклогексанола. Неравенство концентраций кетона и гидроперекиси связано с тем, что перекись водорода расходуется не только в реакции разветвления цепи. [42]
В качестве растворителя для обезмасливания широко применяют двойные и тройные смеси кетонов ( ацетона, метилэтил-кетона и др.) с толуолом или с толуолом и бензолом. Кетон является осадителем парафина, а толуол и бензол - разбавителями масла. С повышением концентрации кетона образуются более крупные, так называемые дендритные кристаллы парафина, которые отфильтровываются от смеси значительно лучше мелких кристаллов. [43]
Последний пример, иллюстрируя положение, что наблюдаемые кинетические соотношения могут изменяться при резком изменении концентраций, показывает также и существенные затруднения при интерпретации кинетических закономерностей реакции на основе ее механизма. Реакция имеет первый порядок по ацетону, однако на самом деле в стадии, определяющей скорость, участвует енол. Концентрация енола пропорциональна концентрации кетона, поскольку енол находится с последним в равновесии. Поэтому говорят, что енол кинетически эквивалентен кетону. Наблюдаемую закономерность для скорости при очень низкой концентрации брома можно интерпретировать так, как если бы ацетон или енол реагировали с бромом, и только другие данные показывают, что с бромом реагирует именно енол. Обычно можно предложить не один механизм, согласующийся с наблюдаемой кинетикой реакции-особенно, если быстрые равновесия делают различные частицы кинетически эквивалентными. [44]
Уменьшение глубины окисления приводит к увеличению выхода циклогексанона в расчете на окислившийся циклогексан. Однако при этом понижается концентрация кетона, что увеличивает расходы на его выделение. В связи с этим целесообразно проанализировать еще один фа-ктор, влияющий на выход промежуточных продуктов - температуру реакции. [45]
Страницы: 1 2 3 4