Концентрация - свободная кислота
Cтраница 1
Концентрация свободной кислоты в ванне зависит от поступления аммиака и подачи свежей кислоты. Количество пропускаемого через сатуратор газа и содержание аммиака в нем являются малоколеблющимися величинами. Следовательно, постоянство кислотности ванны зависит в основном от равномерности подачи кислоты. Поэтому ввод кислоты в сатуратор должен быть равномерным, и содержание свободной кислоты в ванне должно контролироваться самим аппаратчиком не реже чем каждые два часа. [1]
Концентрация свободной кислоты в этом растворе должна быть около 1 5 N и не должна выходить за пределы 1 0 - 2 0 N. Прибавляют 10 мл 2 % - но-го раствора а-бензоиноксима в этаноле. Образовавшийся осадок извлекают три раза порциями ( по 10 мл) хлороформа. Соединение молибдена с а-бензо-иноксимом образует молочнообразную суспензию в СНСЦ. Оставшиеся следы молибдена удаляют добавлением 10 мл 2 % - ного а-бензоиноксима и экстракцией тремя порциями ( по 10 мл) хлороформа. Объединенные молибденовые экстракты промывают два раза порциями ( по 10 мл) 1 5 N НС1О4, которые присоединяют к водному раствору. [2]
Концентрация свободной кислоты в этом растворе должна быть около 1 5 N и не должна выходить за пределы 1 0 - 2 0 N. Прибавляют 10 мл 2 % - но-го раствора а-бензоиноксима в этаноле. Образовавшийся осадок извлекают три раза порциями ( по 10 мл) хлороформа. Оставшиеся следы молибдена удаляют добавлением 10 мл 2 % - ного а-бензоиноксима и экстракцией тремя порциями ( по 10 мл) хлороформа. Объединенные молибденовые экстракты промывают два раза порциями ( по 10 мл) 1 5 N НС1О4, которые присоединяют к водному раствору. [3]
Если концентрация свободной кислоты или высаливающего агента повышается, то оба электролита будут связывать значительное количество реагента ( растворителя) S. При этом, конечно, будет увеличиваться и активность аА -, однако значение знаменателя в уравнении (4.17) также растет, в то время как активность as уменьшается. [4]
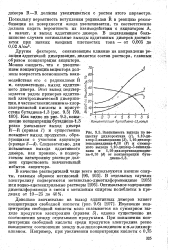
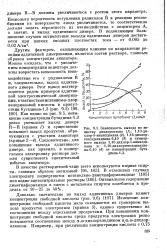
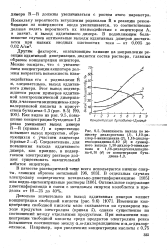
Изменение концентрации свободной кислоты мало сказывается на суммарном выходе продуктов электролиза ( кривая 5), однако существенно на соотношений между отдельными продуктами. При повышении концентрации свободной кислоты среди продуктов электролиза резко повышается соотношение между о & ш-дихлоралкдиеном иа о-дихлор-алканом. [6]
Изменение концентрации свободной кислоты мало сказывается на суммарном выходе продуктов электролиза ( кривая 5), однако существенно на соотношении между отдельными продуктами. При повышении концентрации свободной кислоты среди продуктов электролиза резко повышается соотношение между а со-дихлоралкдиеном и ю-дихлор-алканом. [8]
Изменение концентрации свободной кислоты мало сказывается на суммарном выходе продуктов электролиза ( кривая 5), однако существенно на соотношений между отдельными продуктами. При повышении концентрации свободной кислоты среди продуктов электролиза резко повышается соотношение между а со-дихлоралкдиеном иа о-дихлор-алканом. [10]
Для снижения концентрации свободной кислоты наиболее часто используется метод нейтрализации растворов содой, едкими щелочами, аммиаком и другими реагентами, в результате чего кислота безвозвратно теряется, причем на указанные операции в промышленности расходуются большие количества химических реагентов. [11]
Скорость реакции пропорциональна концентрациям свободной кислоты и амина ( аммиака), которые определяются равновесием диссоциации соли. Константа этого равновесия растет с повышением температуры, чем и обусловлен выбор температуры амидиро-вания. [12]
Скорость реакции пропорциональна концентрациям свободной кислоты и амина ( аммиака), которые определяются равновесием диссоциации соли. Константа этого равновесия растет с повышением температуры, чем и обусловлен выбор температуры амидирования. [13]
В результате этих реакций концентрация свободной кислоты понижается. [14]
Имеется несколько методов определения концентрации свободной кислоты в растворах, основанных на титровании. [15]
Страницы: 1 2 3 4