Концентрация - свободная кислота
Cтраница 3
Поскольку Т Т0 - ус Т0 - ун - г у, то, если известна константа сольватации Кс, из уравнения (3.25) можно найти концентрацию свободной кислоты у. [31]
Такой режим привел к увеличению повреждений труб на некоторых АЭС, где такие повреждения уже имелись, а также одновременно на многих АЭС появилось утонение труб, связанное с концентрацией свободной кислоты. Теоретически это должно было исключить высокие локальные концентрации коррозионно-активных форм фосфатов. Однако повреждения продолжались, особенно на парогенераторах, работавших ранее на фосфатном режиме, даже на тех, где трубки парогенератора перед переходом на гидразино-аммиачный режим тщательно проверялись на отсутствие трещин токами Фуко, а парогенераторы промывались сильными струями воды. [32]
При определениях содержания органических кислот или их солей следует различать: 1) общую кислотность, или общее содержание кислоты, понимая под этим общее количество анионов и недиссоциированных молекул кислоты; 2) концентрацию водородных ионов, часто обозначаемую истинная кислотность; 3) титруемую кислотность; под этим часто понимают концентрацию свободной кислоты. Однако это справедливо только для одноосновных кислот. У двуосновных кислот часть общей кислотности, которую можно титровать щелочью, состоит из двух фракций: недиссоциированной кислоты и одновалентных кислотных ионов. [33]
Процесс ведут при очень интенсивном барботировании. Концентрация свободной кислоты в растворе должна быть не выше 0 5 %, так как при более высокой концентрации происходит интенсивное растворение железа. Понижение концентрации серной кислоты достигается либо разбавлением раствора, либо добавкой известкового молока. Медный шлам, содержащий 60 - 80 % Си, периодически выгружают и отправляют на переплавку. Расход железа составляет примерно 3 кг на 1 кг меди. Процесс рентабелен в больших производствах. [34]
Скорость окисления увеличивается с повышением в растворе концентрации соли железа ( II) и кислорода. Концентрация свободной кислоты имеет сравнительно малое значение, серная кислота несколько замедляет окисление, соляная кислота ускоряет его. Окисление железа ускоряется также некоторыми другими соединениями, например азотной кислотой и более заметно - фтористоводородной кислотой ( стр. [35]
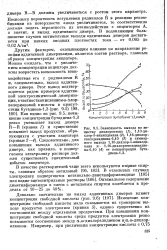
Изменение концентрации свободной кислоты мало сказывается на суммарном выходе продуктов электролиза ( кривая 5), однако существенно на соотношений между отдельными продуктами. При повышении концентрации свободной кислоты среди продуктов электролиза резко повышается соотношение между о & ш-дихлоралкдиеном иа о-дихлор-алканом. [36]
Изменение концентрации свободной кислоты мало сказывается на суммарном выходе продуктов электролиза ( кривая 5), однако существенно на соотношении между отдельными продуктами. При повышении концентрации свободной кислоты среди продуктов электролиза резко повышается соотношение между а со-дихлоралкдиеном и ю-дихлор-алканом. [38]
Изменение концентрации свободной кислоты мало сказывается на суммарном выходе продуктов электролиза ( кривая 5), однако существенно на соотношений между отдельными продуктами. При повышении концентрации свободной кислоты среди продуктов электролиза резко повышается соотношение между а со-дихлоралкдиеном иа о-дихлор-алканом. [39]
На холоду эта реакция протекает медленно, но ускоряется при нагревании. Скорость окисления зависит также и от концентрации свободной кислоты. [40]
Определив X, прибавляют небольшими порциями к исследуемому раствору крепкий раствор слабого основания МОН. При этом, пока происходит уменьшение концентрации свободной кислоты, электропроводность раствора уменьшается. Когда же гидролиз практически нацело подавлен, дальнейшая добавка слабого основания почти не вызывает изменения электропроводности. Таким образом мы имеем все данные, необходимые для расчета степени гидролиза соли. [41]
Определив Я, прибавляют небольшими порциями к исследуемому раствору крепкий раствор слабого основания МОН. При этом, пока происходит уменьшение концентрации свободной кислоты, электропроводность раствора уменьшается. Когда же гидролиз практически нацело подавлен, дальнейшая добавка слабого основания почти не вызывает изменения электропроводности. Измерив электропроводность такого раствора, получим Яс. Таким образом мы имеем все данные, необходимые для расчета степени гидролиза соли. [42]
Определив Я, прибавляют небольшими порциями к исследуемому раствору крепкий раствор слабого основания МОН. При этом, пока происходит уменьшение концентрации свободной кислоты, электропроводность раствора уменьшается. Когда же гидролиз практически нацело подавлен, дальнейшая добавка слабого основания почти не вызывает изменения электропроводности. Измерив электропроводность такого раствора, получим Яс. Таким образом, мы имеем все данные, необходимые для расчета степени гидролиза соли. [43]
Необходимо отметить, что осажденце висмута некоторыми из перечисленных анионов нередко сопровождается образованием небольших количеств основной соли. Загрязнение осадка основной солью увеличивается при уменьшении концентрации свободной кислоты в растворе соли висмута и добавлении очень большого избытка реактива, если последний представляет соль сильного основания и слабой кислоты и, следовательно, имеет щелочную реакцию. [44]
Для определения по номограмме содержания кислоты в травильном растворе точку на шкале удельного веса, соответствующую удельному весу данного раствора, соединяют прямой линией с точкой, соответствующей данному раствору на шкале концентрации соли железа. Точка пересечения этой прямой со шкалой содержания кислоты укажет концентрацию свободной кислоты в данном растворе. [45]
Страницы: 1 2 3 4