Концентрация - слабая кислота
Cтраница 1
Концентрация слабой кислоты увеличивается в 100 раз. Во сколько раз увеличится ( уменьшится) степень диссоциации кислоты. [1]
Если концентрация слабой кислоты в растворе Сд [ НА ] [ А ], а концентрация иона металла Сме [ Ме ], то для данного рН в насыщенном растворе соли МеА, содержащем один из общих ионов, справедливо соотношение: СлСме К ( тв) у. [2]
Варьируя концентрации слабой кислоты и ее соли, удается получить буферные растворы с заданными величинами рН, достаточно устойчивые к внешним воздействиям. [3]
Варьируя концентрацию слабой кислоты и ее соли, удается получить буферные растворы с заданными величинами рН, достаточно устойчивые к внешним воздействиям. [4]
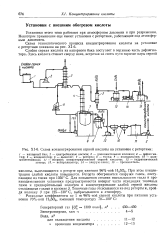 |
Схема концентрирования серной кислоты на установке с ретортами. [5] |
При этом концентрация слабой кислоты повышается. Реторта обогревается снаружи газом, поступающим из топки при 1050 С. Топочные газы отсасываются из-под реторты и, пройдя колонку 3 при 125 - 130 С, выбрасываются в атмосферу. [6]
Если известны концентрация слабой кислоты ( или основания) и численное значение константы диссоциации, легко рассчитать концентрацию ионов водорода и рН раствора. [7]
При вычислении концентрации слабой кислоты, необходимой для растворения заданного числа молей соли другой слабой и к тому же летучей кислоты, приходится учитывать летучесть последней. Точно так же приходится поступать, если дело идет о кислоте, легко распадающейся на воду и летучий ангидрид. [8]
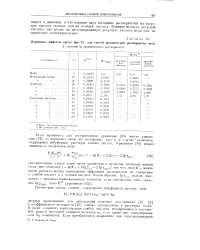 |
Первичные эффекты среды при 25 для смесей органический растворитель-вода. [9] |
В таких элементах концентрация слабой кислоты поддерживается постоянной, равной некоторой заданной величине / j, в то время как концентрация соли пг2 изменяется. [10]
В таких элементах концентрация слабой кислоты поддерживается постоянной, равной некоторой заданной величине тпг, в то время как концентрация соли mz изменяется. [11]
При этом в растворе несколько возрастает концентрация слабой кислоты, которая практически не диссоциирует на ионы. Следовательно, происходит лишь незначительно малое изменение концентрации ионов водорода в растворе. [12]
Область буферирования рН зависит от соотношения концентраций слабой кислоты и сопряженного основа-кия. Обычно колебания этого соотношения не выходят за довольно широкие, но определенные пределы - 10 % кислоты и 90 % основания в смеси, с одной стороны, и 90 % кислоты и 10 % основания, с другой стороны. [13]
Иначе говоря, повышение кислотности раствора ВЫЗЫЕ увеличение концентрации слабой кислоты буферной смеси, а вышение щелочности раствора вызывает повышение концен: ции соли буферной смеси. Однако такое изменение концентра компонентов буферной смеси сравнительно мало отражается величине рН раствора. [14]
Из уравнения реакции гидролиза этой соли видно, что концентрации слабой кислоты и гидроксид-ионов, образующихся в результате гидролиза, равны между собой. [15]
Страницы: 1 2 3 4