Концентрация - неэлектролит
Cтраница 3
Такой метод элиминирования диффузионного потенциала применим лишь тогда, когда сравниваются кислотности близких по составу растворов. Несомненно, что большие различия в ионной силе, рН и концентрациях неэлектролитов оказывают заметное влияние на диффузионный потенциал. [31]
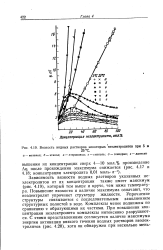
Картина несколько меняется в присутствии многоатомных спиртов. В водных растворах KF и КС1, содержащих этн-ленгликоль, значение Лт ] почти не зависит от концентрации неэлектролита [19] ( рис. 4.17, 4.18), хотя вязкость раствора в исследованном интервале концентрации этиленгликоля повышается при 5 С в 44 раза, при 25 С - в 17 раз. Вязкость же повышается в 4300 раз при 5 С и в 1000 раз при 25 С. Энергия активации вязкого течения растворов с этиленгликолем и глицерином очень незначительно превышает энергию активации проводимости этих растворов. [32]
Эти факты показывают, что влияние гликоля и глицерина на число переноса ионов гидроксила в водных растворах КОН зависит от концентрации неэлектролита. В низкой концентрации гликоль и глицерин снижают долю прототропного механизма в переносе электричества. В растворах с большим содержанием этих неэлектролитов доля прототропной проводимости быстро возрастает, что в этих условиях означает перенос протонов не через молекулы воды, а через молекулы глицерина. Механизм прототропной проводимости через гликоль почти так же эффективен, как через воду, но через глицерин он намного эффективнее. [33]
Целью настоящей работы является установление характера зависимости удельной электропроводности раствора электролита от концентрации неэлектролита, диэлектрической проницаемости раствора и предельной высокочастотной электропроводности растворителя. Значительный интерес представляет изучение этих зависимостей для водно-органических смесей, диэлектрическая проницаемость которых уменьшается ( вода-спирт, вода-ацетон) и увеличивается ( вода - мочевина, вода - тиомочевина) с ростом концентрации неэлектролита. [34]
 |
Истинные т и кажущиеся t числа переноса катионов некоторых электролитов при 25 С. [35] |
Существование рассмотренного эффекта можно легко установить, прибавив к электролиту недиссоциирующее на ионы вещество, например сахар или мочевину. После электролиза концентрация прибавленного неэлектролита ( вычисленная по отношению к воде) окажется по-разному изменившейся у электродов, причем у одного из них она увеличится, а у другого уменьшится. [36]
Основной особенностью этого метода является измерение чисел переноса в растворах электролита, содержащих растворенный неэлектролит ( например, сахар) в первоначально равномерной концентрации. Экспериментальные наблюдения показали, что при электролизе концентрация неэлектролита около электродов изменяется. Неэлектролит, растворенный в жидкости, нейтрален по отношению к действию электрического поля и переносу ионов. [37]
В табл. 1 приведены полученные нами экспериментальные данные по растворимости хлорида, бромида и иодида калия в воднодиоксановых растворителях различного состава при температуре 25 С. Из таблицы видно, что в ряду KJ - КВг - КС1 растворимость солей уменьшается, причем различие в растворимости бромида и хлорида калия в несколько раз меньше по сравнению с растворимостью иодида калия. Характер уменьшения растворимости с добавлением диоксана для всех трех солей однотипен: при концентрациях неэлектролита примерно до 0 2 мольных долей наблюдается более резкое снижение растворимости. При дальнейших добавках диоксана растворимость плавно и незначительно уменьшается: в случае хлорида калия - почти до нуля, а для остальных двух солей до 1 5 ( КВг) и 3 5 ( KJ) г / моль / lOQO г растворителя. Надо отметить, что в изученных системах при температуре 25 С не происходит расслаивания компонентов. [38]
Прогресс в области калориметрических методов, достигнутый за последние 10 - 15 лет, позволил получить в отдельных случаях ошибки в измерении ДЯХ менее 0 01 кДж моль -, а ошибка порядка 0 04 кДж - моль 1 является для растворимых соединений в настоящее время вполне обычной. Для измерений применяют как традиционные ячеечные калориметры, так и проточные. В современных калориметрах можно работать с такими концентрациями растворов, при которых энтальпия растворения в пределах погрешности опыта уже не обнаруживает зависимости от концентрации неэлектролита. Именно это позволило резко повысить точность определяемых значений ДЯ5, так как прежде приходилось прибегать к экстраполяции на бесконечное разведение функций вида ДЯ / 2 или & H / XiX2, где ДЯ - интегральная энтальпия растворения. [39]
Неэлектролиты, подобные ацетону и спиртам, могут быть деионизованы методом, который используется для воды. Эти методы применимы к почти безводным органическим жидкостям я их водным растворам. В первом случае ионы поглощаются смолой медленнее, чем из водных растворов. Концентрация неэлектролитов в начальных порциях фильтрата из ионообменной колонки может отличаться от исходной, так как смолы в присутствии воды могут их сорбировать. Основная электролитическая примесь в низших первичных спиртах и в водном растворе формальдегида - кислота, образовавшаяся в результате окисления этих веществ атмосферным кислородом. Чтобы удалить кислоту, во многих случаях достаточно пропустить раствор через колонку анионообменника в ОН - - форме. [40]
Сорбция увеличивается также при взаимодействии между диполями неэлектролитов и ионами смолы. Высаливающий эффект ионов оказывает противоположное действие. Тем не менее отношение внутренней и внешней концентраций неэлектролитов приблизительно постоянно, по крайней мере в пределах малых концентраций для любых раствора и смолы. [41]
В отношении влияния неэлектролитов на водные растворы электролитов наблюдается значительное различие между электролитами, ионы которых мигрируют чисто гидродинамически, и электролитами, ионы которых переносят электричество и по прототропному механизму. В растворах первых электролитов основной механизм миграции не изменяется под влиянием неэлектролитов; изменяются лишь условия переноса электричества. В растворах ионов с прототропной проводимостью присутствие неэлектролита, особенно в большой концентрации, существенно изменяет механизм переноса электричества. Гидродинамическая миграция может подавить гарототропный механизм проводимости, а природа последнего при повышении концентрации неэлектролита в растворе может измениться, если обмен протонов между молекулами неэлектролита будет преобладать над обменом протонов между молекулами воды. Однако влияние неэлектролитов на про-тотропную проводимость трудно отделить от их влияния на гидродинамическую миграцию отчасти потому, что участвующие в прототропной проводимости ионы оксония мигрируют, также по гидродинамическому механизму, и отчасти потому, что другие ионы электролита переносят электричество также в результате гидродинамической миграции. [42]
 |
Вязкость водных растворов некоторых неэлектролитов при 5 в. [43] |
Зависимость вязкости водных растворов указанных неэлектролитов от их концентрации также имеет максимум ( рис. 4.19), который тем выше и круче, чем ниже температура. Повышение вязкости и наличие максимума означают, что неэлектролит упрочняет структуру жидкости. Упрочнение структуры связывается с последовательным заполнением структурных полостей в воде. Комплексы менее подвижны по сравнению с образующими их частями. При повышении концентрации неэлектролита комплексы интенсивно разрушаются. [44]
Концентрационные коэффициенты растворимости при всех изученных температурах проходят через минимум ( рис. 8, а), смещающийся с повышением температуры в область больших добавок ацетона. Указанный факт, а также уменьшение численных значений dCsm / dX2 с ростом температуры указывает на то, что при повышении температуры влияние добавок ацетона на структуру воды и растворимость аргона менее эффективно. Зависимости Csm f ( X2) для системы вода-ацетамид ( рис. 7, б) симбатны изотермам Csm f ( X2) для водных растворов одноатомных спиртов: имеет место максимум растворимости аргона при Х2 0 005 и слабо выраженный минимум, смещающийся с повышением температуры в область меньших добавок неэлектролита. Причины появления максимума растворимости рассмотрены выше. Следует лишь отметить смещение максимума Csm в область меньших по сравнению с одноатомными спиртами концентраций неэлектролита. Это может быть объяснено более сильным разрушающим действием ацетамида на структуру воды за счет усиления гидрофильной гидратации. [45]
Страницы: 1 2 3 4