Концентрация - окись - азот
Cтраница 1
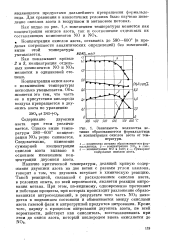 |
Зависимость количества ис. [1] |
Концентрация окиси азота с повышением температуры несколько уменьшается. [2]
Концентрацию окиси азота ( во втором поглотительном приборе) рассчитывают по этой же формуле. [3]
К концентрация окиси азота, необходимая для полного торможения, [ NO ] 1017 см-3. Совпадение результатов расчета с экспериментом очень хорошее. [4]
Уменьшения концентрации окиси азота легко дс ггичь введением небольшого количества кислорода. [5]
Определим концентрацию окиси азота, при которой реакционный объем будет минимальным. [6]
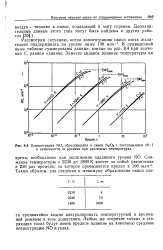 |
Концентрация NO, образующейся в смеси N2 / Oj с соотношением 40. 1 в зависимости от времени при различных температурах. [7] |
Рассмотрим ситуацию, когда концентрацию окиси азота желательно поддерживать на уровне ниже 100 млн-1. В приведенной ниже таблице суммированы данные, взятые из рис. 8.4 при значении С, равном единице. [8]
Вдали от равновесия, когда концентрация окиси азота еще невелика, обратными реакциями ( 2) и ( 3) можно пренебречь. [9]
В зависимости от температуры и концентрации окиси азота и кислорода в газовой фазе устанавливается определенное равновесие между компонентами этой реакции. [10]
С другой стороны, повышение концентрации окиси азота, например, при специальном насыщении ею реакционной смеси приводит к повышению выхода фенилдинитрометана. [11]
 |
Зависимость содержания окиси азота в конечном газе от среднемассовой температуры. [12] |
Опытные данные, характеризующие зависимость концентрации окиси азота ( в пересчете на воздух, смешиваемый с теплоносителем-плазмой) в зависимости от средне-массовой температуры фактически изображаются одной кривой независимо от состава плазмы. [13]
С другой стороны, повышение концентрации окиси азота, например, при специальном насыщении ею реакционной смеси приводит к повышению выхода фенилдинитрометана. [14]
Таблица показывает, что с повышением температуры концентрация окиси азота увеличивается. [15]
Страницы: 1 2 3 4