Концентрация - окись - азот
Cтраница 2
В результате этой работы оказалось, что концентрации окиси азота в воздухе при температурах превращения двуокиси углерода ( до 2100) колеблются между 3 6 и 6 7 об емными процентами. На этом основании было вычислено, что для получения одного килограмма 100 % азотной кислоты необходим расход 7 7 килоуатт-часов. [16]
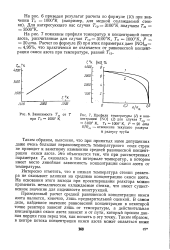 |
Профили температуры ( / и концентрации [ NO ] ( 2 для случая Г 3100 К, Го 1000 К, Р 20 ста RlRm - отношение текущего радиуса к радиусу трубы. [17] |
На рис. 7 показаны профили температур и концентраций окиси азота, рассчитанные для случая 7ср3100оК, Т0 1000 К, Р 20 arm. Расчет по формуле ( 9) при этих параметрах дает [ NO ] cp 4 95 %, что практически не отличается от равновесной концентрации окиси азота при температуре, равной Гер. [18]
Если коксовый газ проходит стадию водной промывки, концентрация окиси азота в нем увеличивается. Это объясняется разложением нитритов аммония 4Л1, присутствующих в оборотной воде в результате жизнедеятельности нитробактерий. [19]
При такой концентрации кислорода, вне зависимости от концентрации окиси азота в исходном газе, имеет место максимальная скорость окисления. [20]
При такой концентрации кислорода, вне зависимости от концентрация окиси азота в исходном газе, имеет место максимальная скорость окисления. [21]
При такой концентрации кислорода, вне зависимости от концентрации окиси азота в исходном газе, имеет место максимальная скорость окисления. [22]
При такой концентрации кислорода, вне зависимости от концентрации окиси азота в исходном газе, имеет место максимальная скорость окисления. [23]
 |
Принципиальная схема установки для изучения кинетики окисления азота. [24] |
На рис. XI.17 показана зависимость от удельной энергии концентрации окиси азота. Энергетические выходы вычислены по формуле (XI.29), которая и в данных условиях сохраняет силу. Как видно, в этом случае при постоянной силе тока уравнение (XI.30) хорошо описывает экспериментальные данные. Второй порядок разложения не дает совпадения. [25]
Таким образом, при малых - должна наблюдаться пропорциональность концентрации окиси азота удельной энергии, действительно наблюдающаяся на опыте. [26]
 |
Пределы взрывчатости аммиака в смесях кислород-азот. [27] |
На практике желательно получать самую высокую из числа воз-можных концентрацию окиси азота, так как при этом для получения данного выхода потребуется аппаратура меньших размеров и будет получаться более крепкая кислота, как это будет показано ниже. Если принять во внимание большое количество азота в тазах, то становится очевидным благоприятный результат замены некоторой части этого инертного газа кислородом. В промышленном масштабе это осуществил Фаузер 535, который добавляет около 4 % кислорода к воздуху и таким образом окисляет смесь газов, содержащую 11 % аммиака. [28]
 |
Принципиальная схема получгния азотной кислоты из N2 и О2 с помощью плазмы под давлением 10 ат. [29] |
При 3200 К и закалке с помощью циркулирующего нитрозного газа концентрация окиси азота в газе составляла 4 %; при этом расход электроэнергии был равен 16 тыс. квт-ч / т NO. [30]
Страницы: 1 2 3 4