Концентрация - окись - азот
Cтраница 3
При эквимолярных смесях азота с кислородом и температуре реакции 3500 С концентрация окиси азота в выхлопном газе турбины будет достигать 6 5 % объемн. [31]
Дальнейшее увеличение содержания кислорода в составе реакционной смеси нецелесообразно ввиду снижения концентрации окиси азота в контактных газах, затрудняющего осуществление второй стадии производства азотной кислоты - абсорбции окислов азота водой. [32]
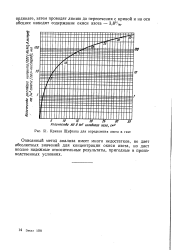 |
Кривая Шуфтана для определения азота в газе. [33] |
Описанный метод анализа имеет много недостатков, не дает абсолютных значений для концентрации окиси азота, но дает вполне надежные относительные результаты, пригодные в производственных условиях. [34]
 |
Эффективность закалки при различных условиях. [35] |
Тнач - температура в начале закалки; ( NO) Ha4 - концентрация окиси азота в начале закалки, равная равновесной концентрации при Гнач: ( NO) KOH - концентрация окиси азота в конце закалки. [36]
Для интенсификации процессов, идущих в абсорбционном отделении, необходимо, чтобы концентрация окиси азота в нитрозных газах была максимальной, что возможно при условии повышения содержания аммиака в исходной газовой смеси или при повышении общего давления. [37]
Это же относится и к оптимальной концентрации кислорода, которая зависит не от концентрации окиси азота, а лишь от состава воздуха, которым разбавляют нитрозные газы. [38]
Рей и Огг рассчитали константу скорости ks и константу равновесия / Сравн - Концентрация окиси азота в этой системе очень низка. Схема реакции дает возможность предположить, что в этих условиях окисление окиси азота катализируется двуокисью азота. Относительно функции двуокиси азота в стадии 3 возникает вопрос: действует ли она как третье тело или же имеет место какой-то химический обмен. [39]
Во-первых, если газ забирают из объема, в котором горит факел, то концентрация окиси азота невелика. [40]
Поскольку окисление окиси азота является одной из наиболее медленно протекающих реакций, большое значение имеет концентрация окиси азота и кислорода в газе. Если в башни к нитрозиым газам добавить воздух, то с повышением концентрации кислорода скорость окисления окиси азота вначале повышается, но это в свою очередь приводит к разбавлению нитрозных газов. Поэтому при большо м количестве добавленного воздуха скорость реакции будет снижаться. [41]
Джемс и Сагден [1007] нашли, что интенсивность этого спектра пропорциональна концентрации атомов О и концентрации добавляемой окиси азота. [42]
Поскольку окисление окиси азота является одной из наиболее медленно протекающих реакций процесса, большое значение имеет концентрация окиси азота и кислорода в газе. [43]
Поскольку окисление окиси азота является одной из наиболее медленно протекающих реакций процесса, большое значение имеет концентрация окиси азота и кислорода в газе. Если в башни к ни-трозным газам добавить воздух, с повышением концентрации кислорода скорость окисления окиси азота вначале повышается, но это в свою очередь приводит к разбавлению нитрозных газов. [44]
Как видно из опытных данных, концентрация кислорода в исходной смеси в значительной мере влияет как на концентрацию окиси азота в конечном газе, так и на энергетический выход окиси азота. Экспериментальная зависимость концентрации окиси азота от содержания кислорода в исходной смеси отлична от теоретической, что объясняется недостаточным смешением реагирующих компонентов. [45]
Страницы: 1 2 3 4