Концентрация - исходный продукт
Cтраница 3
Это означает, что произведение равновесных концентраций конечных продуктов реакции в 1 000 000 раз меньше произведения концентраций исходных продуктов реакции. [31]
К основным факторам, оказывающим решающее влияние на ход химического процесса, прежде всего относятся температура, давление и концентрация исходных продуктов. [32]
Если скорость обратной реакции существенно ( например, на несколько порядков) меньше скорости прямой реакции, то при равновесии концентрации исходных продуктов будут близки к нулю, так что данную реакцию можно рассматривать как практически необратимую. Например, при сгорании метана в кислороде Д1040, что говорит о том, что данная реакция необратимая. [33]
Если К равно 106, то это означает, что произведение концентрация конечных продуктов реакции в 1 000 000 раз больше произведения концентрации исходных продуктов реакции. [34]
Если К равно 10е, то это означает, что произведение концентраций конечных продуктов реакции в 1 000 000 раз больше произведения концентраций исходных продуктов реакции. [35]
Пусть и - концентрация молекул наиболее медленно реагирующего с исходным активного промежуточного продукта ( например, атомов Н в приведенной выше схеме), а с - концентрация всего исходного продукта, который реагирует по бимолекулярной схеме с активными молекулами промежуточного продукта. [36]
Пусть и - концентрация активного промежуточного продукта ( например, атома водорода, как в приведенной выше схеме), наиболее медленно реагирующего с исходными, ас - концентрация всего исходного продукта, который реагирует по бимолекулярной схеме с активными молекулами промежуточного продукта. [37]
Следовательно, для уменьшения и предотвращения реакций уплотнения процесс надлежит вести при более высоких давлениях водорода, но увеличение концентрации водорода при реакции дегидрирования будет сдвигать равновесие в сторону возрастания концентрации исходных продуктов. Поэтому выбор давления водорода должен быть ограничен определенными пределами, при которых в найденных температурных условиях давление водорода не препятствовало бы ароматизации сырья. [38]
Исследованиями ряда авторов [ 7-и ] было показано, что при взаимодействии растворов солей кадмия ( нитраты, сульфаты, хлориды) с аммиаком сначала идет обменная реакция с выделением гидроокисных осадков различного состава ( основные соли и основные аммиакаты) в зависимости от концентрации исходных продуктов и их молекулярных отношений. Последующее добавление аммиака приводит к растворению осадков и образованию растворимых комплексных аммиакатов. В системе CdS04 - NH3 - Н20 образование гидроокиси кадмия возможно лишь в очень разбавленных растворах - 0.005 мол. [39]
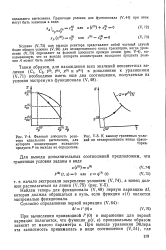 |
Фазовая плоскость реак - [ IMAGE ] - 5. К выводу граничных уело. [40] |
Условие ( V73) для выхода реактора представляет собой частный случай более общего условия ( V, 20) для незакрепленного конца траектории, когда уравнение ( V, 73) определяет на фазовой плоскости прямую линию ( рис. V-4), показывающую, что на выходе аппарата концентрация исходного продукта реакции А может быть любой. [41]
Определение кинетических параметров реакции ( 1) обычными методами представляет большую трудность, так как она протекает очень быстро и практически до конца. Снятие кинетических кривых изменения концентрации исходного продукта аммиака возможно в узких пределах, поскольку дальнейшее повышение содержания МН3 может привести к взрыву аммиачно-воздушных и аммиачно-кислородных смесей. [42]
Страницы: 1 2 3