Концентрация - перекисный радикал
Cтраница 3
При этом предполагают [38, 39], что хемилюминесценция в видимой и ультрафиолетовой областях спектра возбуждается за счет энергии, выделяющейся при рекомбинации перекисных радикалов. Ослабление хемилю-минесцентного свечения происходит из-за уменьшения концентрации активных перекисных радикалов, которые взаимодействуют с присутствующими ингибиторами, образуя малоактивные радикалы ингибиторов. [31]
Последняя зависит от соотношения скоростей образования и гибели свободных радикалов. Следовательно, для управления процессом окисления следует научиться уменьшать концентрацию перекисных радикалов. На этом основан механизм действия различных добавок, приводящих в итоге к замедлению окисления, о чем будет указано ниже. [32]
Чем больше константа скорости этой реакции ( k7), тем меньшее количество ингибитора необходимо использовать для уменьшения скорости процесса на одну и ту же величину. Однако определение абсолютного значения k7 весьма за -, труднительно, так как концентрация перекисных радикалов в системе обычно не известна. В связи с этим для определения эффективности ингибитора пользуются относительными константами k7 / kz и k7 [ Yk6, которые при окислении одного и того же вещества в стандартных условиях могут служить количественными характеристиками активности ингибитора. [33]
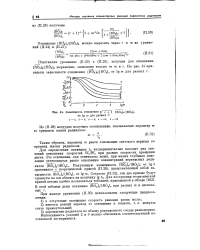 |
Зависимость отношения у г ( [ R02 ] o / [ ROs ] s. [34] |
Это отношение, как отмечалось выше, при малых глубинах окисления углеводорода равно отношению концентраций перекисных радикалов [ R02 ] 0 / [ R62 ] S. Согласно (11.32), эти две кривые будут сдвинуты по оси абсцисс на величину Ig гц. [35]
В присутствии ингибиторов различных классов ( фенолов, аминов и др.) скорость окисления падает за счет уменьшения концентрации перекисных радикалов, ведущих цепи окисления. Конкретный механизм действия ингибитора зависит от его природы, свойств окисляемого углеводорода, условий проведения реакции. [37]
Как было только что показано, в одинаковых условиях в присутствии данного ингибитора интенсивность свечения количественно характеризует относительную концентрацию перекисных радикалов. Чем более активен ингибитор, тем меньшая концентрация ингибитора необходима для того, чтобы уменьшить в определенное число раз концентрацию перекисных радикалов, а, следовательно, и интенсивность свечения. [38]
Методом кислородного последействия [280- 283], так же как и методом фотохимического последействия, определяются константы скорости рекомбинации радикалов по кинетике установления стационарного режима, регистрируемой по хемилюминес-ценции. Различие состоит в методе получения нестационарной концентрации радикалов. В методе кислородного последействия нестационарная концентрация перекисных радикалов создается путем быстрой подачи кислорода в систему, состоящую из вещества, способного к окислению, инициатора и активатора. [39]
При полном отсутствии кислорода рекомбинируют только радикалы R. Поскольку константа скорости реакции R 02 очень велика 1, то уже при сравнительно малых концентрациях кислорода углеводородные радикалы полностью превращаются в перекисные и рекомбинируют только перекисные радикалы. Дальнейшее повышение концентрации кислорода на концентрацию перекисных радикалов уже не влияет. [40]
Действие ингибиторов неразрывно связано с цепным механизмом реакций окисления. Окисление органических соединений осуществляется при участии перекисных радикалов. Скорость окисления W kz [ RH ] [ R02 ]; она определяется концентрацией перекисных радикалов. [41]
Действие ингибиторов неразрывно связано с цепным механизмом реакций окисления. Окисление органических соединений осуществляется при участии перекисных радикалов. Скорость окисления W / г2 [ RH ] [ R02 ]; она определяется концентрацией перекисных радикалов. [42]
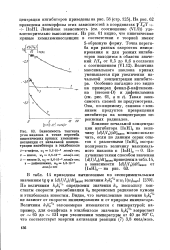 |
Зависимость тангенса угла наклона в точке перегиба кинетических кривых хемилюминесценции от начальной концентрации ингибитора в этилбензоле. [43] |
Точка перегиба при разных скоростях инициирования и для разных ингибиторов находится в области значений / / / от 0 5 до 0 6 в согласии с соотношением ( VI. Величина максимального наклона кривых уменьшается при увеличении начальной концентрации ингибитора. Такая зависимость схемой не предусмотрена. Она, по-видимому, связана с влиянием продуктов превращения ингибитора на концентрацию перекисных радикалов. [44]
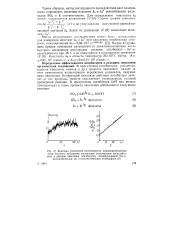
Газ, содержащий радикалы, до поступления на узел вымораживания, направлялся предварительно в съемные обогреваемые реакторы. На рис. 11 показано изменение концентрации радикалов в зависимости от температуры. Были использованы реакторы с насадкой, обработанные борной кислотой, тетраборатом калия, бромистым барием, хлористым калием, бромистым калием, и необработанный реактор. Между тем в реакторе, обработанном КС1, она уменьшалась ( кривая 5), начиная с 8 ( Г С. Начало рекомбинации на других поверхностях, как видно из рисунка, лежит в промежутке между 80 и 350 С. Сохранение концентрации перекисных радикалов неизменной вплоть до 350 С в реакторе, обработанном борной кислотой, не укладывается в представление об изомеризации и распаде их с энергией активации пусть даже равной 25 ккал. [45]
Страницы: 1 2 3