Концентрация - равновесный раствор
Cтраница 1
Концентрация равновесного раствора, при которой в адсорбционном слое образуются двумерные ассоциаты гемимицелл, может быть названа критической концентрацией двумерной поверхностной ассоциации. Обозначим ее символом С ( р) асс. [1]
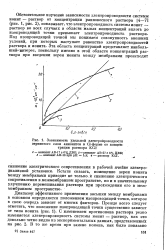 |
Зависимость удельной электропроводности зернистого слоя анионитов в Cl-форме от концентрации раствора KG1. [2] |
Обстоятельное изучение зависимости электропроводности системы ионит - раствор от концентрации равновесного раствора [4-7] ( рис. 1, рис - 2), показывает, что электропроводность системы ионит - раствор во всех случаях в области малых концентраций вплоть до изопроводящей точки превышает электропроводность раствора. Под изопроводящей точкой мы понимаем совокупность внешних условий, при которых наступает равенство электропроводностей раствора и ионита. [3]
Величина Е зависит от вида ионита, природы и концентрации равновесного раствора и колеблется от 2 до 7 ккал / молъ. [4]
Таким образом, для нахождения активности растворителя вместо определения давления пара измеряют концентрацию равновесных растворов обычным аналитическим методом. [5]
Максимальная плотность заполнения гидрофобной поверхности углеродных адсорбентов ионами ПАВ достигается в том случае, если концентрация равновесного раствора приближается к критической концентрации мицеллообразования. [6]
Поэтому в работах, посвященных распределению, обязательно следует указывать рН, температуру, диапазон концентраций равновесных растворов, способ определения равновесных концентраций и другие условия проведения анализа. [7]
 |
Графическая интерполяция хорд равновесия по методу Шервуда. [8] |
Для корреляции опытных данных и облегчения их интерполяции предложены различные способы графического изображения зависимости между концентрациями равновесных растворов. Желательно, чтобы указанные зависимости были для всех систем линейными. В этом случае экстраполяция экспериментальных данных облегчается и при наличии только двух хорд равновесия можно находить положение всех остальных. [9]
Анионы многоосновных кислот НПХ образуют противоионы от Шя Х ] до Х - в зависимости от концентрации равновесного раствора кислоты или ее кислой соли. [10]
Как видно из рисунка, рассчитанные изотермы адсорбции по двум - трем экспериментальным величинам адсорбции, определенной вблизи эквимолекулярной концентрации равновесного раствора с использованием модели регулярного раствора, удовлетворительно согласуются с экспериментальными данными. [11]
На рис. 1 представлены изотермы адсорбции стекловолокном исследованных модификаторов в координатах: количество граммов модификатора на один грамм стекловолокна - концентрация равновесного раствора в молях на литр. [13]
 |
Схема структуры элементарного пакета хризотил-асбеста. [14] |
В случае баженовского асбеста адсорбция силикат-иона во внутренней обкладке двойного электрического слоя приводит сначала к нейтрализации положительного заряда волокна, а с повышением концентрации равновесного раствора - к перезарядке поверхности волокна и увеличению абсолютной величины отрицательного заряда поверхности. [15]
Страницы: 1 2 3
