Концентрация - равновесный раствор
Cтраница 3
Это уравнение определяет геометрическое место точек пересечения рабочих линий и соответствует прямой линии с углом наклона, равным - DF / Ap. Линия отсекает на оси ординат отрезок JF / AF, на оси абсцисс - отрезок JF / DF и пересекает кри - вую равновесия в точке с координатами ( vp, yF), соответствующей концентрациям равновесного раствора на ступени питания. [31]
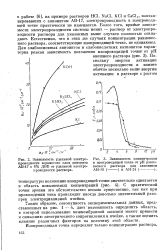
NaCl, KC1 и СаС13, контактировавших с анионитом АВ-17, электропроводность в изопроводящеи точке практически не изменяется. Более того, крийые зависимости электропроводности системы ионит - раствор от электропроводности раствора для указанных выше случаев полностью совпадают. Естественно, что в этих не случаях концентрации равновесного раствора, соответствующие изопроводящеи точке, не одинаковы. [33]
 |
Зависимость удельной электропроводности мембран анкалит К-2 с разным отношением СФС. ТП от концентрации равновесного раствора хлористого натрия. [34] |
Многие физико-химические и эксплуатационные свойства ионитов, как, например, механическая прочность, способность к поглощению ионов, срок службы и другие, зависят от их гомогенности. Однако в настоящее время не существует простых и быстрых способов оценки степени гомогенности. Ранее [1 ] было показано, что при уменьшении концентрации разбавленного равновесного раствора неоднородность материала ионита должна приводить к резкому падению его электропроводности. [35]
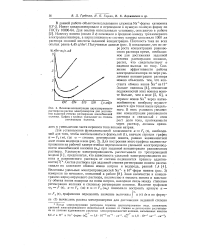 |
Влияние концентрации циркулирующего раствора на расход электроэнергии для достижения заданной степени регенерации ионообменной колонки. Цифры у кривых указывают на степень регенерации колонки. [36] |
В данной работе объектом исследования служила Na - форма катионита КУ-2. Полученные данные ( рис. 1) показывают, что по мере роста концентрации равновесного раствора время, необходимое для достижения заданной степени рагенерации колонки, растет, что свидетельствует о падении выхода по току. Снижение эффективности работы электродиализатора по мере увеличения концентрации раствора можно объяснить тем, что константа обмена ионов КГа на Н больше единицы [4], отношение подвижностей этих ионов в иони-те больше, чем в воде [5, 6], а перенос ионов Na через катио-нообменную мембрану осуществляется при токах выше предельного. В этих условиях увеличение концентрации равновесного раствора и связанный с этим рост доли тока, протекающего через раствор, должны приводить к уменьшению части переноса тока ионами натрия. [37]
При этом измерялось количество адсорбата, введенное в колонну с известной массой адсорбента. Рассчитывались интегралы, соответствующие исправленным временам, удерживания разных доз ( концентраций) адсорбируемого вещества [ см. уравнение (7.34) ] и площадям соответствующих пиков, и находились адсорбция и концентрация равновесного раствора с. [38]
Эта неоднородность состоит в том, что фиксированные ионы распределены по всему объему ионита не равномерно, а сосредоточены в гелевых участках, отделенных друг от друга межгелевыми промежутками. Последние практически не содержат фиксированных ионов и заполнены равновесным раствором. Негомогенность материала ионита приводит к тому, что в области разбавленных равновесных растворов с увеличением их концентрации электропроводность ионита сильно возрастает. Такой характер зависимости электропроводности ионита от концентрации равновесного раствора может быть количественно объяснен с точки зрения модельных представлений, которые сводятся к следующей схеме. Гелевые участки, где содержатся почти все фиксированные ионы, имеют сравнительно высокую электропроводность. Межгелевые промежутки заполнены равновесным раствором, удельная электропроводность их отвечает этому раствору. [39]
Поскольку адсорбция - экзотермический процесс, повышение температуры должно вызывать уменьшение адсорбции. Действительно, это всегда наблюдается при физической адсорбции газов и паров. При адсорбции из растворов не меньшую роль играет, однако, и то, как температура влияет на растворимость вещества и, следовательно, на величину химического потенциала его в равновесном растворе. В соответствии с этим одной и той же концентрации равновесного раствора с ростом температуры должны отвечать различные величины в или концентрации адсорбированного вещества. Если растворимость вещества с повышением температуры увеличивается, адсорбция должна уменьшаться; при падении растворимости с нагреванием раствора адсорбция будет увеличиваться. [40]
Между тем в последние годы появился более совершенный материал, оказавшийся пригодным для моделирования линейно поляризующихся электродов - ионообменные мембраны. Однородность ионитовых мембран достаточно высока. Удельное сопротивление гетерогенных мембран растет по мере уменьшения относительного содержания ионообменной смолы и увеличения количества связки. Кроме того, р зависит от природы противоиона, определяющего форму мембраны, и концентрации равновесного раствора. Таким образом, удельное сопротивление ионообменных мембран можно варьировать в очень широких пределах: резкие изменения р получают, меняя количество ионита в мембране, плавные - изменением формы мембраны и концентрации равновесного раствора. [41]
В данной работе объектом исследования служила Na - форма катионита КУ-2. Полученные данные ( рис. 1) показывают, что по мере роста концентрации равновесного раствора время, необходимое для достижения заданной степени рагенерации колонки, растет, что свидетельствует о падении выхода по току. Снижение эффективности работы электродиализатора по мере увеличения концентрации раствора можно объяснить тем, что константа обмена ионов КГа на Н больше единицы [4], отношение подвижностей этих ионов в иони-те больше, чем в воде [5, 6], а перенос ионов Na через катио-нообменную мембрану осуществляется при токах выше предельного. В этих условиях увеличение концентрации равновесного раствора и связанный с этим рост доли тока, протекающего через раствор, должны приводить к уменьшению части переноса тока ионами натрия. [42]
Между тем в последние годы появился более совершенный материал, оказавшийся пригодным для моделирования линейно поляризующихся электродов - ионообменные мембраны. Однородность ионитовых мембран достаточно высока. Удельное сопротивление гетерогенных мембран растет по мере уменьшения относительного содержания ионообменной смолы и увеличения количества связки. Кроме того, р зависит от природы противоиона, определяющего форму мембраны, и концентрации равновесного раствора. Таким образом, удельное сопротивление ионообменных мембран можно варьировать в очень широких пределах: резкие изменения р получают, меняя количество ионита в мембране, плавные - изменением формы мембраны и концентрации равновесного раствора. [43]
Зауер и Рупперт, изучая влияние гидрофильных коллоидов на скорость основного обмена, применили другой метод. Величину нагрузки, соответствующую точно 50 % - ному обессоливанию, определяли интерполяцией и использовали как сравнительную. Результаты, полученные по методам, служащим для измерения скоростей ионообменных процессов, а также по последнему названному методу зависят и, возможно, даже в значительной мере от размера и однородности зерен фильтрующего материала и его упаковки в колонке. Возможно, что поэтому метод не нашел широкого применения. Определение скорости обмена при нейтральном обмене затрудняется ( поскольку нужно проводить очень много определений величины жесткости объемным методом в области средних концентраций жесткости) из-за отсутствия надежных и быстрых методик определения концентрации равновесного раствора. [44]
Жидкостная адсорбционная хроматография ( ЖАХ) основана на различии в константах равновесия системы компонент в растворе - адсорбент для разделяемых компонентов раствора. Теория селективности ЖАХ должна основываться на теории адсорбции из бинарных и более сложных жидких растворов. Из-за отсутствия количественной теории разбавленных растворов, а тем более адсорбции из растворов, коэффициенты активности компонентов раствора в адсорбированном состоянии и константы равновесия определяют из экспериментальных изотерм адсорбции. Энергия адсорбции веществ из растворов определяется разностью энергий межмолекулярного взаимодействия его молекул с адсорбентом и с соседними молекулами со стороны объема раствора, поэтому она может быть в несколько раз меньше энергии адсорбции того же компонента из газовой фазы. Жидкостная хроматография может быть использована для изучения адсорбции из растворов и определения константы Генри и изотермы адсорбции из растворов тремя путями. Во-первых, константа Генри и изотерма адсорбции из растворов, особенно в области весьма малых концентраций, могут быть определены из самих хроматограмм адсорбата ( положительно адсорбирующееся вещество из разбавленных растворов) при элюи-ровании из колонны, заполненной исследуемым адсорбентом, растворителем. В-третьих, жидкостная хроматография на аналитических колоннах ( с тем же или другим адсорбентом) может быть использована в качестве вспомогательного аналитического метода для определения концентраций равновесных растворов над изучаемым адсорбентом при статических определениях изотермы адсорбции, когда равновесие заведомо достигается. [45]
Страницы: 1 2 3