Концентрация - равновесный раствор
Cтраница 2
Среднерастворимая соль CaSO4 - 2H2O ( гипс) и малорастворимые карбонаты MgCO3 и СаСОз, а также фосфаты кальция, железа и алюминия переходят в вытяжку частично в зависимости от состава и концентрации равновесного раствора. [16]
Таким образом, решение задачи, возникающей на последней ступени конкретизации термодинамического описания - расчета коэффициентов активности, может быть полезным и при решении прикладных задач, в качестве одного из этапов оценки селективности ионита при изменении концентрации равновесного раствора. [17]
Цель данного сообщения - на примере исследованных нами равновесий обмена ионов щелочных металлов на протон на сульфо-катионите КУ - 2X8 в сульфатных и хлоридных растворах - показать, как влияют взаимодействия ионов в фазах раствора и ионита на величину коэффициента селективности ионита при увеличении концентрации равновесного раствора. [18]
Зависимость / Ср от Cs определяется тангенсом угла наклона касательной к кривой, выражающей зависимость CR / CS. С уменьшением концентрации равновесного раствора / Ср увеличивается. [19]
В противоположность сильноосновному аниониту АВ-17 слабоосновный анионит ЭДЭ-10П в гидроксильной форме имеет низкую электропроводность, особенно в области разбавленных равновесных растворов, что связано, вероятно, с малой степенью диссоциации слабых оснований. Однако при увеличении концентрации равновесного раствора едкого кали электропроводность смолы резко возрастает. Подобная картина имеет место и в случае слабокислотного катионита КБ-4-2П, когда равновесным раствором является соляная кислота. Оба равновесных раствора - едкое кали и соляная кислота - обладают аномально высокой электропроводностью. Поэтому небольшое увеличение их количества в ионите за счет адсорбции должно приводить к большему увеличению электропроводности, чем в случае, например, хлористого натрия. [21]
Расхождение между ними определяет степень отклонения от подчинения системы правилу Здановского. Эта погрешность возрастает с уменьшением концентрации равновесного раствора. [22]
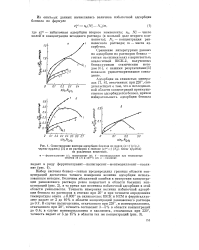 |
Сопоставление изотерм адсорбции бензола из паров ( af ( plps. [23] |
Величина абсолютной ошибки в измерении концентрации равновесного раствора резко возрастает в области больших концентраций ( рис. 2), в то время как величина избыточной адсорбции в этой области уменьшается. [24]
Действительно, предположением, достаточным для объяснения этих особенностей, является гипотеза, что резинаты с принадлежащей им при данной активности растворителя водой набухания и необменно поглощенные электролиты образуют практически несмешивающиеся системы. Количество воды, вошедшее при этом с электролитами, задается концентрацией равновесного раствора. [25]
Ксантогенат целлюлозы, как и другие вещества, способен образовывать пересыщенные растворы. Под степенью пересыщения понимают отношение концентрации в пересыщенном растворе, находящемся в неравновесном метастабильном состоянии, к концентрации равновесного раствора. Для вискозных растворов в связи с химической нестабильностью ксантогената можно лишь приблизительно ( по косвенным данным) оценить возможную степень пересыщения при формовании. Ксантогенат целлюлозы, по-видимому, неограниченно смешивается с водным раствором едкого натра. Однако концентрации не превышают 12 - 16 % из-за чрезмерно больших вязкостей. На основании полученных результатов ( см. раздел 7.2.2) установлено, что рН10 - 12 на поверхности волокна достигается в течение 0 01 с. За этот промежуток времени осаждения не происходит и, следовательно, образуется пересыщенный раствор. [26]
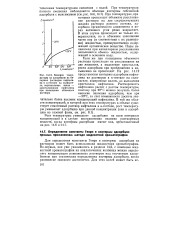 |
Влияние температуры на адсорбцию из бинарных растворов нафталина в и-гептане на силикаге-ле. вертикальные линии - кристаллизация нафталина при насыщении объемного раствора. [27] |
Для определения константы Генри и изотермы адсорбции из растворов может быть использована жидкостная хроматография. Во-первых, как уже указывалось в разделе 14 2, с помощью жидкостной хроматографии на аналитических колоннах можно определять концентрации равновесных растворов над изучаемым адсорбентом при статических определениях изотермы адсорбции, когда равновесие заведомо достигается. [28]
Решение вопросов разделения ионов и регенерации ионообменных смол в колонках при наложении постоянного тока требует знания удельной электропроводности различных солевых форм ионитов. В настоящей работе по ранее разработанной методике [2] исследована зависимость удельной электропроводности ионитов АВ-17, ЭДЭ-10П и КБ-4-2П от природы, температуры и концентрации равновесного раствора. Предварительные опыты показали, что для гарантированного перевода любой из применявшихся смол из одной формы в другую через ячейку достаточно пропустить в течение 10 - 12 час. [29]
Если сравнить эти два раствора, полученные различными способами, через промежуток времени, меньший чем т, то их концентрации будут отличаться друг от друга. Но можно с уверенностью сказать, что сколько бы времени этот раствор ни стоял, его концентрация не будет ниже кривой 2 и выше кривой 1, и что значение концентрации равновесного раствора будет лежать между значениями концентраций этих двух растворов. [30]
Страницы: 1 2 3
