Концентрация - реагирующее вещество
Cтраница 1
Концентрации реагирующих веществ увеличиться от этого не могут. Следовательно, константа скорости данной реакции является действительно постоянной величиной только при заданной температуре. Как бы мы ни меняли концентрации веществ А и В, константа скорости от этого не меняется; она, следовательно, не зависит от концентраций реагирующих веществ. [1]
Концентрации реагирующих веществ у наружной поверхности зерен в этом случае близки к равновесным, порядок реакции близок к первому и наблюдаемая энергия активации очень мала. Вследствие относительно медленного переноса тепла реакции, темп - pa поверхности катализатора в этом случае отличается от темп-ры реакционной смеси и для экзотермич. Во внешне-диффузионной области протекают промышленные реакции окисления аммиака, окисления спиртов, поверхностного горения. В этой области активность катализатора не влияет на наблюдаемую скорость реакции, а лишь определяет границы условий осуществления реакции в области внешней диффузии. [2]
Концентрация реагирующих веществ также влияет на равновесие; осаждение бывает более полным при наличии небольшого избытка осадителя. [3]
Концентрации реагирующих веществ у внешней поверхности пористого катализатора весьма близки к концентрациям их в объеме, концентрации же в порах падают от наружной поверхности зерен пористого катализатора к их центру, а концентрации продуктов реакции соответственно возрастают. Кинетика процесса при этом зависит от соотношения внешней и внутренней поверхности; если они соизмеримы, то кинетика соответствует промежуточной области. [4]
Концентрации реагирующих веществ на поверхности катализатора и в объеме равны, но реакции протекают только на внешней поверхности катализатора, не захватывая внутренней поверхности. Кинетика процесса при этом определяется кинетикой химической реакции. [5]
Концентрация реагирующих веществ оказывает сильное влияние на выход целевых продуктов, что видно из уравнения для определения / Ср любой реакции. [6]
Концентрация реагирующих веществ оказывает влияние на скорость реакции всех типов ( кроме реакций нулевого порядка): с увеличением концентрации исходных реагентов скорость реакции возрастает. [7]
 |
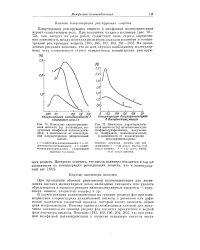
Зависимость скорости реакции горения от времени. [8] |
Концентрация реагирующих веществ с течением времени падает, так как в ходе реакции количество исходных веществ уменьшается. Кривая / ( рис. 77) выражает характер изменения скорости изотермической реакции от времени. Реакции горения характеризуются большим выделением теплоты. При отсутствии теплоотвода это приводит к увеличению температуры реагирующих веществ. [9]
Концентрация реагирующих веществ NH3 и О2 влияет на скорость процесса окисления NH3 и выход NO. При повышении температуры границы взрывоопасное расширяются. [10]
Концентрация реагирующего вещества у свободной поверхности слоя весьма близка к концентрации в объеме: С 5 st C0; концентрация же в порах спадает практически до нуля. Эту область можно назвать областью диффузии в порах, или, согласно весьма удачному предложению Вулиса, внутренней диффузионной областью. [11]
Концентрации реагирующих веществ возводятся в степени доказанных стехиометрических коэффициентов, отражающих механизм элементарных актов реакции. [12]
Концентрации реагирующих веществ увеличиваются подачей в доменную печь природного газа, основной компонент которого метан. [13]
Концентрации реагирующих веществ у наружной поверхности зерен в этом случае близки к равновесным, порядок реакции близок к первому и наблюдаемая энергия активации очень мала. Вследствие относительно медленного переноса тепла реакции, темп - pa поверхности катализатора в этом случае отличается от темп-ры реакционной смеси и для экзотермич. Во внешне-диффузионной области протекают промышленные реакции окисления аммиака, окисления спиртов, поверхностного горения. В этой области активность катализатора не влияет на наблюдаемую скорость реакции, а лишь определяет границы условий осуществления реакции в области внешней диффузии. [14]
Страницы: 1 2 3 4