Концентрация - сульфит
Cтраница 1
Концентрация сульфита 0 2 М, мочевины 8М, На оси ординат отложено количество ( моль) сульфгидрильных групп, освободившихся на 1 моль соединения. [1]
Концентрацию сульфита устанавливают иодометрически. [2]
Концентрацию сульфита натрия рассчитывают по формуле обратного титрования. Так как растворы сульфита натрия поглощают углекислый газ, а также легко окисляются, рекомендуется работать со свежеприготовленным раствором. [3]
С - концентрация сульфита натрия, г / л; О, - расход сульфита натрия с момента установления постоянного дефицита кислорода, л / ч; 7 88 - стехиометрический коэффициент. [4]
Прямое определение имеет преимущество при концентрации сульфитов, равной или превышающей 0 5 мг / л, и при отсутствии мешающих веществ. Колориметрически с фуксином сульфиты определяются после удаления двуокиси серы из подкисленной пробы и поглощения ее раствором едкого натра. [5]
При этом в процессе аэрации концентрация сульфита натрия уменьшается линейно во времени в очень широком диапазоне концентраций. [6]
Повторите опыт, но изменяйте концентрацию сульфита натрия так же, как это было сделано для растворов йодата натрия. [7]
В качестве параметров смеси, аддитивно зависящих от концентрации сульфита, выбраны при этом оптические свойства пульпы. Относительная приведенная погрешность измерения концентрации MgO в диапазоне 4 - 8 % nMgSO3 в диапазоне 7 - 12 % составляет не более 2 % при изменении дисперсности частиц от 100 до 300 мкм. [8]
В качестве параметров смеси, аддитивно зависящих от концентрации сульфита, выбраны при этом оптические свойства пульпы. Относительная приведенная погрешность измерения концентрации MgO в диапазоне 4 - 8 % nMgSOs в диапазоне 7 - 12 % составляет не более 2 % при изме - нении дисперсности частиц от 100 до 300 мкм. [9]
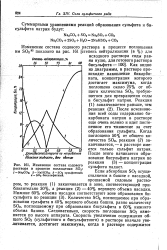 |
Изменение состава содового раствора в процессе поглощения SO2. [10] |
После этого начинается образование бисульфита натрия по реакции ( 3) - концентрация сульфита падает. [11]
Используя методику определения содержания Na2SO3 в котловой воде с повышенной чувствительностью, автор показал, что конденсат, отобранный из турбины, обладает кислой реакцией и восстановительными свойствами, находящимися в прямой зависимости от концентрации сульфита в котловой воде; изменения содержания Na2SO3 в котловой воде непосредственно влияли на величину рН конденсата. [12]
В согласии с этим механизмом обмен идет между S - S36O3 и SO3, но не между S35 - SO3 и SO3 Эмис и Уилард [724] изучили кинетику этого обмена и нашли, что скорость его пропорциональна произведению концентраций сульфита и тиосульфата. Это исключает диссоциацию последнего на S SO3 -, как путь обмена. Обмен тиосульфата с HS35 - сульфидов идет медленнее, чем с сульфитом, однако оба имеют одинаковую энергию активации [718], что можно объяснить общей медленной ступенью разрыва связи S - SB комплексе. [13]
В несколько колб наливают по 15 мл приготовленных стандартных растворов, прибавляют по 10 мл свежеприготовленного реактива и через 30 мин измеряют оптическую плотность, вычитают значения ее для холостого определения и строят график зависимости оптической ( плотности от концентрации сульфита. [14]
KQI, к02, Е, R, ть т2 - постоянные коэффициенты, получаемые расчетом и в эксперименте; G0i - количество поступающего в аппарат сульфита-сушенки, кг / ч; V0 - расход топлива, кг / ч; CQI, с02 - концентрации сульфита и сульфата магния в поступающем продукте, гмоль / кг; с2, Сз - концентрация сульдита и сульфата магния в огарке, гмоль / кг; с0з - содержание влаги в исходном материале, %; В - вес ванны кипящего слоя, кг; т - время; С - теплоемкость ванны кипящего слоя, ккал / кг град. [15]
Страницы: 1 2 3 4