Концентрация - адсорбтиво
Cтраница 3
Математическая модель термодесорбционного процесса позволяет проследить за изменением концентрации адсорбтива в каждой точке объема цилиндра, заполненного цеолитом, и температуры его нагрева. На рис. 2 - 48 в качестве примера показано ( для С0 0 03 кг / м3) изменение концентрации углекислого газа в процессе термодесорбции в выходном сечении цилиндра Сотв, выходные кривые среднеинтегральной концентрации Ск и температуры внутренней поверхности адиабатического десорбера. Для удобства сравнения концентрация Сотв представлена в половинном масштабе. [31]
Значение адсорбции 1 г угля находят по разности концентраций адсорбтива в растворе до и после адсорбции. [32]
С ( т) - средняя по высоте слоя концентрация адсорбтива в газе; гт - удельная теплоемкость адсорбента. [33]
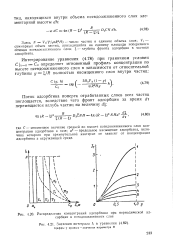 |
Распределение концентраций адсорбтива при периодической адсорбции в псевдоожиженном слое.| Значения интеграла 1 в уравнении. Цифры у кривых - значения параметра В. [34] |
С - мгновенное значение средней по высоте псевдоожиженного слоя концентрации адсорбтива в газе; а - предельное насыщение адсорбента, величина которого при прямоугольной изотерме не зависит от концентрации адсорбтива в окружающей среде. [35]
Зависимость молекулярной равновесной адсорбции из раствора на твердом теле от концентрации адсорбтива характеризуется изотермой адсорбции и для достаточно разбавленных растворов выражается уравнением Фрейндлиха или уравнением Ленгмюра. [36]
С ( т) - усредненная по объему шаровой частицы концентрация адсорбтива. [37]
Для построения рабочей линии процесса из уравнения материального баланса находим концентрацию адсорбтива в адсорбенте на выходе из адсорбера. [38]
Форма кривой проскока зависит от большого числа факторов: температуры, концентрации адсорбтива в газе-носителе во входном потоке, адсорбента, его количества или высоты слоя, а также постепенного снижения емкости адсорбента, вызванного закоксо-выванием полостей, истиранием адсорбента и, как следствие, увеличением перепада давления по слою, загрязнением адсорбента другими сопутствующим веществами. Все это может привести к изменению зоны массообмена и кривой проскока. [39]
Эта кривая имеет два прямолинейных участка при малых и больших значениях концентрации адсорбтива. Для аналитического описания изотермы адсорбции было предложено несколько уравнений. Наиболее простым уравнением изотермы адсорбции является уравнение Бедеккера - Фрейндлиха. Бедеккер, а затем Фрейндлих сделали допущение, что изотерма адсорбции является параболой. [40]
Для определения количества адсорбированного вещества необходимо экспериментально найти давление газа или концентрацию адсорбтива в сосуде, в котором происходит адсорбция, до и после адсорбции. Очень часто количество адсорбированного вещества определяют по привесу адсорбента. Следует заметить, что определение количества адсорбированного вещества вызывает часто большие трудности, всегда имеющие место, когда малая искомая величина является разностью двух больших измеряемых величин. Чтобы уменьшить ошибку измерений, определение обычно проводят, применяя в качестве адсорбента пористые тела с большой удельной поверхностью, связывающие поэтому большое количество адсорбтива. Однако это в свою очередь имеет тот недостаток, что на адсорбции может сказываться диаметр пор адсорбента. [41]
Для определения количества адсорбированного вещества необходимо экспериментально найти давление таза или концентрацию адсорбтива в сосуде, в котором происходит адсорбция, до и после адсорбции. Очень часто количество адсорбированного вещества определяют по привесу адсорбента. Следует заметить, что определение количества адсорбированного вещества вызывает часто большие трудности, всегда имеющие место, когда малая искомая величина является разностью двух больших измеряемых величин. Чтобы уменьшить ошибку измерений, определение обычно проводят, применяя в качестве адсорбента пористые тела с большой удельной поверхностью, связывающие поэтому большое количество адсорбтива. Однако это в свою очередь имеет тот недостаток, что на адсорбции может сказываться диаметр пор адсорбента. [42]
С - концентрация вещества после адсорбции; m - масса адсорбента от концентрации адсорбтива в растворе. [43]
Приведенный пример показывает, что доля адсорбированного вещества сильно убывает с повышением концентрации адсорбтива. Следовательно, связывание вещества путем адсорбции наиболее полно происходит при малых концентрациях его. Этим часто пользуются на практике. Например, при получении высокого вакуума остатки воздуха удаляют путем адсорбирования его углем. Так же можно достаточно полно извлекать путем адсорбции растворенные вещества из растворов слабой концентрации. Выгодность применения адсорбции при больших концентрациях адсорбтива понижается. [44]
Крутой подъем начальной части изотермы говорит о том, что небольшое повышение концентрации адсорбтива в начальных стадиях процесса сопровождается сильным увеличением адсорбции. С дальнейшим повышением концентрации рост адсорбции замедляется и, наконец, совершенно приостанавливается: адсорбция достигает предельного максимального значения и дальше уже не зависит от концентрации. [45]
Страницы: 1 2 3 4