Концентрация - экстрагент
Cтраница 4
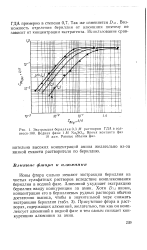 |
Экстракция бериллия 0 3 М раствором ГДА в сол. [46] |
ГДА примерно в степени 0.7. Так же изменяется DAL Возможность отделения бериллия от алюминия поэтому не зависит от концентрации экстрагента. [47]
К - термодинамическая константа равновесия экстракции; ав - активность извлекаемой соли в водной фазе; S - концентрация экстрагента в органической фазе; ys и ус - коэффициенты активности экстрагента и сольвата в органической фазе. [48]
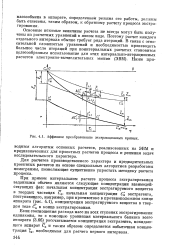 |
Аффинное преобразование экстракционных кривых. [49] |
Если соотношения расхода масс на всех ступенях экстрагирования одинаковы, то с помощью уравнения материального баланса всего аппарата (3.66) рассчитывается концентрация экстрагента, покидающего аппарат Ск и таким образом определяется избыточная концентрация 0, необходимая для расчета первого интервала. [50]
Число молекул органического растворителя и воды, координированных к иону гидроксония, зависит от концентрации кислоты в водной фазе и концентрации экстрагента в органическом разбавителе. [51]
Еще большее различие между этими параметрами наблюдается при экстракции ТБФ ( см. рис. 3), причем р не зависит от концентрации экстрагента, за исключением 5 - 10 % - ных растворов ТБФ. [52]
А ] - концентрация аниона в водной фазе; 5 0 и ( S - дгру) - начальная и равновесная концентрации экстрагента. [53]
А ] - концентрация аниона в водной фазе; S0 и ( S0 - q py) - начальная и равновесная концентрации экстрагента. [54]
 |
Распределение о-фе-ннлфенола ( ОРР в водную фазу при экстракции цезия 1М раствором ОРР в дннзопропил-бензоле. [55] |
Снижение значений D с увеличением концентрации NaOH выше 0 4 моль / л также объясняется [11] образованием фенолята натрия, который снижает концентрацию свободного экстрагента. Образование относительно водорастворимого фенолята натрия может привести к значительным потерям фенола с водной фазой. Возможно, столь резкое увеличение растворимости связано с мицеллообразова-нием соответствующего фенолята в водном растворе. [56]
Таким образом, коэффициент разделения двух элементов определяется константами комплексообразования их с экстрагентом и с анионами в водном растворе, а также концентрацией экстрагента в органической фазе. Сопоставляя эти константы для скандия с одноименными величинами для тория и циркония ( табл. 4), видим, что наиболее благоприятной средой для разделения скандия и тория являются азотнокислые растворы, а для разделения пары скандий-цирконий - солянокислые растворы. С целью увеличения коэффициента разделения элементов необходимо, чтобы в процессе экстракции сохранялась высокая концентрация анионов в водном растворе. [57]
Коэффициент распределения уранила между растворами ди-н-бутилфосфорной кислоты в толуоле и водными растворами азотной кислоты обратно пропорционален квадрату концентрации Н - ионов и прямо пропорционален квадрату концентрации экстрагента. [58]
Практически во всех опубликованных работах не рассматривается обратимость реакции ( исследуется область, далекая от равновесия), а экстракция производится в таких условиях, что концентрация экстрагента, а следовательно, и анионов дитизона или других кислот в водной фазе остается постоянной. Последнее условие имеет место при экстракции микроколичеств элемента М растворами с относительно высокой концентрацией экстрагента, а также других веществ, влияющих на скорость экстракции. [59]
Страницы: 1 2 3 4