Концентрация - гидроксид-ион
Cтраница 3
При добавлении к воде кислоты возрастает концентрация ионов водорода и снижается концентрация гидроксид-ионов за счет образования недиссоциированных молекул воды. [31]
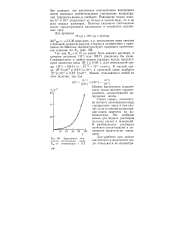 |
Зависимость константы диссоциации воды Kv от температуры t ( LC. [32] |
Это означает, что увеличение концентрации водородных ионов вызывает соответствующее уменьшение концентрации гидроксид-ионов, и наоборот. Равновесие между ионами Н и ОН существует не только в чистой воде, но и во всех водных растворах. Поэтому указанное соотношение может характеризовать кислотность и основность различных сред. [33]
Это означает, что увеличение концентрации водородных ионов вызывает соответствующее уменьшение концентрации гидроксид-ионов, и наоборот. Равновесие между ионами Н и ОН существует не только в воде, но и во всех водных растворах. Поэтому указанное соотношение может характеризовать кислотность и основность различных сред. [34]
В чистой воде ( в нейтральной среде) концентрация ионов водорода равна концентрации гидроксид-ионов. Прибавление к воде кислоты увеличивает концентрацию ионов водорода и соответственно снижает концентрацию гидроксид-ионов. Произведение же их концентраций ( точнее активностей) сохраняет постоянное значение, равное ионному произведению воды. [35]
При добавлении к воде кислоты концентрация катионов водорода Н увеличивается, а концентрация гидроксид-ионов ОН - в соответствии с принципом Ле Шателье убывает. При добавлении к воде щелочи концентрации ионов изменяются в обратном направлении. Ионное же произведение воды независимо от изменения концентраций ионов остается при неизменной температуре постоянным. Постоянство ионного произведения воды позволяет вычислять концентрацию ОН по числовому значению концентрации Н, и наоборот. [36]
При работе гальванического элемента у поверхности катодных участков в воде происходит повышение концентрации гидроксид-ионов. Под действием растворенного в воде кислорода происходит окисление этого соединения до гидроксида железа ( III): 4Ре ( ОН) 2 О2 2Н2О4Ре ( ОН) 3, который образует рыхлый осадок. [37]
Так как образующееся в результате гидролиза основание представляет собой сильный электролит, то концентрация гидроксид-ионов в растворе превалирует и реакция среды щелочная. Таким образом, соль сильного основания слабой кислоты гид-ролизуется с увеличением концентрации гидр оксид-ионов в растворе. [38]
Так как в раствор кислота и щелочь введены в эквивалентных количествах, то концентрации гидроксид-ионов и молекул НСЮ равны друг другу. [39]
Прибавление к воде кислоты увеличивает концентрацию ионов водорода, в связи с чем концентрация гидроксид-ионов убывает, и наоборот. [40]
Если концентрация сильного основания больше чем 1 - Ю-6 моль / л, то концентрацией гидроксид-ионов вследствие ионизации воды можно пренебречь и принять, что [ ОН - ] СА. [41]
Для определения реакции среды достаточно сведений о концентрации ионов водорода ( рН), а сведениями о концентрации гидроксид-ионов не пользуются. [42]
Ионное произведение воды позволяет для любого водного раствора при известной концентрации ионов водорода [ № 1 найти концентрацию гидроксид-ионов [ ОН - ], и наоборот. [43]
Эти примеры показывают, что если концентрация ионов водорода в водном растворе известна, то тем самым определена и концентрация гидроксид-ионов. [44]
Страницы: 1 2 3