Концентрация - гидроксил-ион
Cтраница 2
Показано, что взаимодействие металла с исходным раствором приводит к нарастанию концентрации гидроксил-ионов в растворе. Скорость и величина этого нарастания определяется природой и состоянием поверхности металла, составом среда. [16]
 |
Нуклеофильная активность и основность важнейших нуклеофильных реагентов. [17] |
Щелочные сульфиды пригодны для дегазации ОВ типа зарин только потому, что они повышают концентрацию гидроксил-ионов в водных растворах. [18]
 |
Зависимость логарифма скорости растворения аморфного кремнезема от рН. ( Данные Баумана. [19] |
Наклон пунктирной линии показывает, что в интервале рН 3 - 5 скорость растворения-приблизительно пропорциональна концентрации гидроксил-ионов. [20]
Бауман [154] показал, что в интервале рН 3 - 6 скорость растворения растет пропорционально концентрации гидроксил-ионов. Следовательно, между значениями рН 0 1 и 3 0 должен быть небольшой минимум, который остался незамеченным. [21]
Такое соотношение отражает наиболее часто встречающуюся ситуацию, когда SH является очень слабой кислотой, а концентрация гидроксил-ионов не настолько велика, чтобы превратить заметную долю SH в S - даже при достижении равновесия. Поскольку [ S - ] в этом случае всегда мала, наблюдаемую константу скорости можно вычислить в обычном приближении стационарного состояния. [22]
НЕЙТРАЛИЗАЦИЯ - химический процесс, направленный на получение нейтрального раствора, в котором концентрация ионов водорода равна концентрации гидроксил-ионов. [23]
Если предположить, что в нашем случае уравнения ( 1) и ( 2) справедливы, то концентрацию гидроксил-ионов можно определять с помощью рН - метра. [24]
Напротив, опуская первую реакцию и включая в число уточняемых параметров константу последней реакции, получаем возможность учитывать систематическую ошибку в калибровке цепи через концентрацию гидроксил-ионов, что важно для исследования весьма слабых кислот Бренстеда ( сопряженные основания для которых имеют среднюю силу) в щелочной области. [25]
Если производить осаждение из горячего раствора, то осаждается чистый карбонат бария, но в присутствии едкой щелочи осадок окклюдирует основные соли и в тем большем количестве, чем выше концентрация гидроксил-ионов в растворе. Метод Винклера, по мнению этих авторов, дает хорошие результаты только тогда, когда осаждение производится из горячего раствора, практически не содержащего других веществ, кроме нормального карбоната натрия. Для этого перед нагреванием раствора следует почти нейтрализовать в нем едкую щелочь соляной кислотой, требуемое количество которой предварительно определяют в отдельной аликвотной части раствора пробы. [26]
Судьба этих ионов различна: гидроксил-ионы не вступают ни в какие реакции, остаются свободными и концентрация их поэтому возрастает; ионы водорода тотчас расходуются на образование уксусной кислоты, и, следовательно, их концентрация будет меньше концентрации гидроксил-ионов. Те ионы водорода, которые возникают и тотчас исчезают, играют роль как бы промежуточного продукта и не войдут в итоговое уравнение. [27]
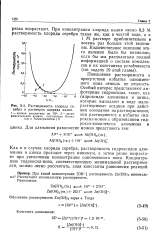 |
Растворимость хлорида серебра в растворах хлорида калия. [28] |
Как и в случае хлорида серебра, растворимость гидроксидов алюминия и цинка проходит через минимум, а затем резко возрастает при увеличении концентрации одноименного иона. Концентрацию гидроксил-иона, соответствующую минимальной растворимости, можно легко рассчитать, зная константы равновесия реакций. [29]
Другим, хотя и менее строгим, является следующее рассмотрение. Известно, что концентрация гидроксил-иона влияет на скорость 5 2 -, но не 5 1-реакции. [30]
Страницы: 1 2 3 4