Различная концентрация - электролит
Cтраница 1
 |
Разрушение эвтектического сплава. а - селективное. б - интеркристаллитное. [1] |
Различные концентрации электролита могут вызывать коррозию, создавая пару даже с одинаковыми металлами ( уравнение Нернста, стр. Различные содержания кислорода также приводят к образованию гальванической пары - менее окисленный и более окисленный металл. [2]
 |
Водородная ( а и кислородная ( б деполяризация при коррозии стали.| Коррозия стали под неподвижной каплей воды. [3] |
Различные концентрации электролита могут вызвать коррозию, создавая пару даже с одинаковыми металлами ( уравнение Нерн-ста, гл. Различное содержание кислорода также приводит к образованию гальванической пары - менее окисленный и более окисленный металл. [4]
 |
Водородная ( а и кислородная ( б деполяризация при коррозии железа.| Коррозия стали под неподвижной каплей воды. [5] |
Различные концентрации электролита могут вызвать коррозию, создавая пару даже с одинаковыми металлами ( уравнение Нернста, гл. Различные содержания кислорода также приводят к образованию гальванической пары - менее окисленный и более окисленный металл. [6]
&x const и различным концентрациям поверхностно-неактивного электролита фона, пересекаются. [8]
Имеются последовательно соединенные ванны с различной концентрацией одинакового электролита. [9]
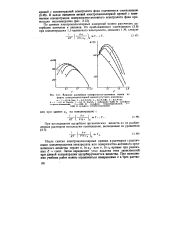 |
Влияние адсорбции поверхностно-активных ионов / на форму электрокапиллярной кривой ртутного электрода. [10] |
После снятия электрокапиллярных кривых в растворах с различными концентрациями электролита или поверхностно-активного органического вещества строят о, In а - или о, In сА - кривые при различных Е - const. Затем определяют угол наклона этих зависимостей пр ( и данной концентрации - адсорбирующегося вещества. [11]
Электрохимические цепи, состоящие из идентичных электродов с различной концентрацией электролитов, называются концентрационными цепями. [12]
С другой стороны, константы электролитической диссоциации слабых электролитов постоянны для различных концентраций электролитов. [13]
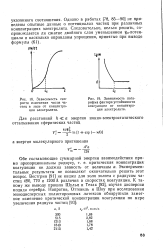
Для подтверждения проведенных рассуждений сопоставим температурные зависимости относительной скорости релаксации при различных концентрациях электролита в растворах перхлората натрия и хлорида цезия. Обе эти соли характеризуйся высокой растворимо-ртью, обе составлены из ионов, один из которых при комнатной температуре является отрицательно гидратируемым, другой - слабо положительно гидратируемым. [14]
 |
Зависимость скорости изменения числа частиц в золе от концентрации электролита.| Зависимость логарифма фактора устойчивости коагуляции от концентрации электролита. [15] |
Страницы: 1 2 3 4
