Различная концентрация - электролит
Cтраница 4
Пусть, например, т коагулируемого латекса измеряется через 1 мин после введения электролита. Назовем эту величину минутной мутностью и обозначим ее т мии. На рис. 39 представлены экпериментальные кривые кинетики коагуляции латекса при различных концентрациях электролита. [46]
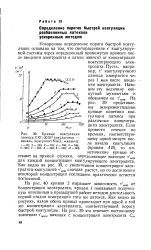 |
Кривые коагуляции латекса СКС-ЗОАР ( эмульгатор - некаль, коагулянт NaCl, ммоль / л. [47] |
Пусть, например, т коагулируемого латекса измеряется через 1 мин после введения электролита. Назовем эту величину минутной мутностью и обозначим ее т мин. На рис. 39 представлены экпериментальные кривые кинетики коагуляции латекса при различных концентрациях электролита. Если провести сечение по в ремени, соответствующему одной минуте после начала коагуляции ( прямая АБ), то кинетические кривые отсекают на прямой отрезки, определяющие значение т мин для каждой концентрации коагулирующего электролита. Как видно на рис. 39, с увеличением концентрации электролита-коагулянта т мин сначала растет, но по достижении некоторой концентрации последнего практически остается постоянной. [48]
Уравнения (11.137) и (11.138) учитывают специфическую адсорбцию только противононов. Таким образом, теория Штерна (11.138) и теория Гуи - Чепмена (11.132) позволяют рассчитать соответственно заряд в плотном и диффузном слоях. Рассчитанные с учетом этих уравнений значения емкости двойного электрического слоя для различных концентраций электролитов удовлетворительно совпадают с результатами, полученными по данным электрокапиллярных измерений. [49]
Глюкауф и Уотте [23] показали, что уравнение ( 3) плохо согласуется с экспериментальными данными. По их мнению, это несоответствие следует отнести за счет неоднородности смолы. Они полагают, что различные партии смолы имеют зерна с неодинаковым числом поперечных связей, а следовательно, разные величины w и Мг и поэтому различные концентрации поглощенного электролита. При выводе уравнения ( 4) предполагалось, что смола имеет одинаковое число поперечных связей. [50]
Наименьшее падение устойчивости при малых добавках электролита наблюдается у дисперсий палыгорскита. Благодаря особенностям кристаллического строения этого минерала, вытянутой планковидной форме его частиц, образующих контакты сцепления в основном лишь по своим углам и ребрам, а также в результате относительно низкой емкости обмена сжатие диффузного слоя не приводит к сколько-нибудь существенной агрегативной коагуляции системы. Таким образом, малая роль электрического фактора устойчивости в электролитсодержащих дисперсиях этого минерала как раз и является причиной преимущественной ( по сравнению с другими, даже солеустойчивыми, но имеющими высокую емкость обмена минералами) устойчивости палыгорскита при самых различных концентрациях электролита в дисперсионной среде. [51]
ПО) и теория Гун - Чепмена ( II. Рассчитанные с учетом этих уравнений значения емкости двойного электрического слоя для различных концентраций электролитов удовлетворительно совпадают с результатами, полученными по данным электрокапиллярных измерений. [52]
 |
Коагулирующие концентрации некоторых электролитов ( ммоль / л для коллоидного раствора сернистого мышьяка ( 7 54 ммоль As2S3 в 1 л. [53] |
Опытные данные показывают, что при повышении концентрации электролита толщина диффузного слоя уменьшается. С этим связано уменьшение и - потенциала. В табл. 62 приведены ( - потенциалы отрицательно заряженного золя сульфида мышьяка при различных концентрациях электролитов - хлоридов калия, бария и алюминия. [54]
Страницы: 1 2 3 4