Поверхностная концентрация - вещество
Cтраница 1
Поверхностная концентрация вещества представляет собой избыток числа молей вещества в некотором объеме раствора вблизи поверхности ( 1 ел. [1]
Можно вычислить поверхностную концентрацию вещества, определяя объем, в котором находится одна молекула 63 1 / CN, где С - концентрация, в моль / см3; N - число Авогадро. [2]
Можно вычислить поверхностную концентрацию вещества, определяя объем, в котором находится одна молекула 631 / CW, где С - концентрация, в моль / см3; N - число Авогадро. [3]
Результатом такого нелинейного соотношения между поверхностной концентрацией вещества и экстинкцией оказывается тот факт, что одно и то же количество вещества при распределении на большей поверхности поглощает сильнее, нежели на меньшей. Высокие поверхностные концентрации неблагоприятны для оценки. [4]
В этих уравнениях 6А и 9в - поверхностные концентрации веществ А и В, выраженные в долях поверхности, занятой этими веществами; СА и CB - их концентрации в газовой фазе; 2& сг - - сумма из произведений адсорбционных коэффициентов всех присутствующих веществ, включая А и В, на их объемные концентрации. [6]
 |
Зависимость Igft. or 1 / 7 для ге-терогенно-каталитических реакций. [7] |
Скорость гетерогенно-каталитического процесса в соответствии с уравнением (111.81) прямо пропорциональна поверхностной концентрации вещества. [8]
Обозначения в системе уравнений ( 7) следующие: SA - поверхностная концентрация вещества А ( например, молекул водорода), причем S без штриха относятся к центрам К, a S - к К; S и S - общее число центров типа К и К па единицу поверхности; S 0 и S0 - то же для незанятых центров; В, С, Н W. [9]
Скорость гетерогенного химического процесса согласно основному постулату химической кинетики прямо пропорциональна поверхностной концентрации веществ. [10]
 |
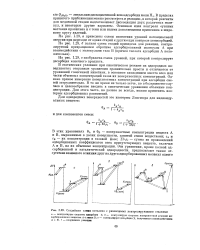
Поляризационные анодные и катодные кривые, отвечающие замедленной химической стадии, в координатах / / реакц-1 ( п lg / / / реакц - ц ( б. [11] |
При замедленных гетерогенных химических стадиях равновесный потенциал электрода и перенапряжение определяются поверхностной концентрацией вещества. Когда поверхностная концентрация потенциалопределяющего вещества достаточно мала и справедлива изотерма Генри, будет наблюдаться прямо пропорциональная зависимость между поверхностной и объемной концентрациями и будут применимы уравнения, полученные для случая замедленной гомогенной химической стадии. [12]
Согласно основному постулату химической кинетики, скорость гетерогенного химического процесса прямо пропорциональна поверхностной концентрации веществ. [13]
Согласно основному постулату химической кинетики, скорость гетерогенной химической реакции прямо пропорциональна поверхностной концентрации вещества. [14]
Согласно основному постулату химической кинетики, скорость гетерогенного химического процесса прямо пропорциональна поверхностной концентрации веществ. [15]
Страницы: 1 2 3