Исходная концентрация - реагент
Cтраница 1
Исходные концентрации реагентов разные. [1]
 |
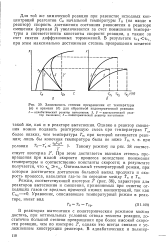
Зависимость концентрации [ IMAGE ] Зависимость концентрации бу-бутандикарбоновых кислот в реак - тандикарбоновых кислот в реакционной. [2] |
При сравнении опытов с разными исходными концентрациями реагентов или условиями проведения следовало учесть, что выходы 3-пентеновой кислоты в этих опытах могут быть различны. [3]
Для обычно применяемой в анализе исходной концентрации реагентов - 25 мкМ скорость реакции образования дитизонатов очень велика. Скорость реакции зависит от органического растворителя и главным образом от рН водного раствора. При хорошем перемешивании фаз ( энергичном встряхивании) для растворов с рН 7 равновесие устанавливается в течение нескольких секунд. В присутствии анионов, способных связывать металл в комплексное соединение ( винная и лимонная кислоты и др.), реакция образования дитизонатов замедляется, что приводит и к уменьшению скорости экстракции. В области рП 4 скорость образования дитизонатов ионов металлов, способных еще к этой реак ции в этих условиях ( Ag, Hg2, Pd2, Pt2, Au3, Cu2, а также Bi3), очень различна. Равновесие для каждого данного иона устанавливается тем медленнее, чем меньше рН водного раствора. [4]
Для учета разбавления раствора при титровании исходные концентрации реагентов должны быть умножены на поправочный коэффициент VHcx / ( VHcx - t - V), где Уиох - исходный объем раствора для титрования, V - объем добавленного титранта. Постоянство рК см) остается вполне удовлетворительным. Полученные таким же путем при других значениях ионной силы величины р / Сзсом) приведены ниже. [5]
 |
Условия определения состава методом молярных отношений с переменной концентрацией металла. [6] |
Пороговые значения рН уменьшаются с ростом исходной концентрации реагента. [7]
В квадратных скобках с индексом О указаны исходные концентрации реагентов, без индекса - концентрации через время t после начала реакции. [8]
Для той же химической реакции при равенстве исходных концентраций реагентов Си начальной температуры Тн ( на входе в реактор) скорость достижения состояния равновесия в реакторе смешения ( прямая 2) увеличивается за счет повышения температуры и соответственно константы скорости реакции, а также за счет снятия диффузионных торможений. [10]
Ас - изменение кон-дентрации реагента; с0 - исходная концентрация реагента; Ах - изменение степени превращения в реакторе; р - плотность жидкости, в которой идет реакция; С. [11]
 |
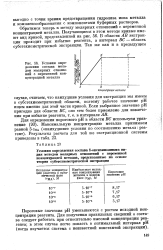
Зависимость gkz от диэлектрической проницаемости е растворителя. [12] |
Кинетика реакции изучалась спектрофотометрически при разных температурах и варьировании исходных концентраций реагентов в присутствии десятикратного избытка галогенид-аниона. [13]
 |
Зависимость давления метилизонитрила от времени. На рисунке показаны два последовательных периода полупревращения для реакции перегруппировки, описываемой уравнением. [14] |
Отметим, что tl / 2 не зависит от исходной концентрации реагента. Это означает, что если измерить концентрацию реагента в произвольный момент времени протекания реакции первого порядка, то спустя время, равное 0 693 / / с, концентрация реагента уменьшится вдвое. Понятие периода полупревращения широко используют при описании радиоактивного распада ядер ( в этом случае его называют периодом полураспада), которое будет подробно рассмотрено в разд. [15]
Страницы: 1 2 3 4